题目内容
【题目】利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品﹣3PbOPbSO4H2O (三盐),主要制备流程如下:
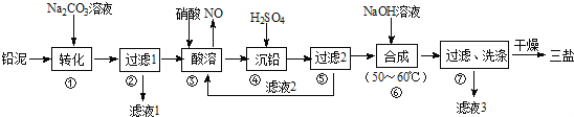
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为______________.
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为______________(写化学式).
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为______________;滤液2中溶质主要成分为______________(写化学式).
(4)步骤⑥合成三盐的化学方程式为______________.
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是______________.
【答案】(1)CO32﹣+PbSO4=PbCO3+SO42﹣(2)Na2SO410H2O(或Na2SO4)
(3)3Pb+8H++2NO3﹣=3Pb2++2NO↑+4H2O HNO3
(4)4PbSO4+6NaOH=3Na2SO4+3PbOPbSO4H2O+2H2O
(5)取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全
【解析】
试题分析:向铅泥中加入Na2CO3溶液,PbSO4转化为难溶PbCO3的离子方程式为CO32-+PbSO4=PbCO3+SO42-,然后过滤得到滤液1为Na2SO4溶液,向滤渣中加入硝酸酸溶,PbO、Pb、PbCO3都与硝酸反应生成 Pb(NO3)2,Pb与硝酸反应还生成NO,铅与硝酸生成Pb(NO3)2及NO的离子方程式为3Pb+8H++2NO3-=3Pb+2NO↑+4H2O,然后向溶液中加入硫酸,生成bSO4沉淀,过滤,滤液2的主要成分是HNO3,向滤渣中加入NaOH溶液,发生反应4PbSO4+6NaOH=3Na2SO4+3PbOPbSO4H2O+2H2O,过滤洗涤干燥得到3PbOPbSO4H2O,滤液3中含有Na2SO4,
(1)通过以上分析知,碳酸钠和硫酸铅发生难溶物的转化,离子方程式为CO32-+PbSO4=PbCO3+SO42-;
(2)通过以上分析知,滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为Na2SO410H2O(或Na2SO4);
(3)通过以上分析知,该离子反应方程式为3Pb+8H++2NO3-=3Pb+2NO↑+4H2O,滤液2中主要成分是未反应的HNO3;
(4)该反应方程式为4PbSO4+6NaOH=3Na2SO4+3PbOPbSO4H2O+2H2O;
(5)该沉淀吸附的离子是硫酸根离子,用盐酸酸化的氯化钡检验,其检验方法为取少量最后一次的洗涤过滤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全。