题目内容
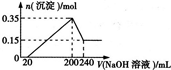 某研究小组将一定质量的镁铝合金材料投入200mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n(mol)与加入NaOH溶液的体积V(mL)的变化如图所示.
某研究小组将一定质量的镁铝合金材料投入200mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n(mol)与加入NaOH溶液的体积V(mL)的变化如图所示.请回答下列问题:
(1)该合金材料中,镁、铝的物质的量之比为
3:4
3:4
(2)硫酸的物质的量浓度为
2.5mol/L
2.5mol/L
.(3)另取相同质量的该合金材料与7.8gNa2O2一起投入足量的H2O中,最终产生的气体在标准状况下的体积为
7.84L
7.84L
.分析:(1)根据图象知,n[Mg(OH)2]为0.15mol,n[Mg(OH)2]+n[Al(OH)3]=0.35mol,则n[Al(OH)3]=0.2mol,根据原子守恒计算镁和铝的物质的量之比;
(2)当沉淀最大时,镁离子和铝离子全部转化为Mg(OH)2、Al(OH)3,溶液中的溶质是Na2SO4,根据氢氧化钠的物质的量计算硫酸的物质的量浓度;
(3)过氧化钠和水反应生成氧气,铝和氢氧化钠反应生成氢气,根据过氧化钠、铝的量计算生成气体的体积.
(2)当沉淀最大时,镁离子和铝离子全部转化为Mg(OH)2、Al(OH)3,溶液中的溶质是Na2SO4,根据氢氧化钠的物质的量计算硫酸的物质的量浓度;
(3)过氧化钠和水反应生成氧气,铝和氢氧化钠反应生成氢气,根据过氧化钠、铝的量计算生成气体的体积.
解答:解:(1)根据图象知,当加入240mLNaOH时,未溶解的固体就是氢氧化镁,则n[Mg(OH)2]为0.15mol,沉淀最多时,沉淀为氢氧化镁和氢氧化铝,n[Mg(OH)2]+n[Al(OH)3]=0.35mol,则n[Al(OH)3]=0.2mol,根据原子守恒得,n(Mg)=n[Mg(OH)2]=0.15mol,n(Al)=n[Al(OH)3]=0.2mol,
所以镁和铝的物质的量之比=0.15mol:0.2mol=3:4,
故答案为:3:4;
(2)氢氧化钠溶液体积200-240mL时,氢氧化钠和氢氧化铝反应Al(OH)3+NaOH=NaAlO2+2H2O,根据方程式知,C(NaOH)=
=5mol/L,
当沉淀最大时,镁离子和铝离子全部转化为Mg(OH)2、Al(OH)3,溶液中的溶质是Na2SO4,
根据硫酸钠的化学式得
n(NaOH)=n(H2SO4),所以c(H2SO4)=
=2.5mol/L,
故答案为:2.5mol/L;
(3)过氧化钠和水反应生成氧气和氢氧化钠,反应方程式为2Na2O2+2H2O=4NaOH+O2↑,根据方程式知,生成n(NaOH)=
×4=0.4mol,生成氧气体积=
×1×22.4L/mol=1.12L,
铝和氢氧化钠反应生成氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据方程式知,0.2mol完全溶解需要n(NaOH)=0.2mol<0.4mol,所以氢氧化钠过量,则生成氢气体积=
×3×22.4L/mol=6.72L,
所以生成气体体积=1.12L+6.72L=7.84L,
故答案为:7.84L.
所以镁和铝的物质的量之比=0.15mol:0.2mol=3:4,
故答案为:3:4;
(2)氢氧化钠溶液体积200-240mL时,氢氧化钠和氢氧化铝反应Al(OH)3+NaOH=NaAlO2+2H2O,根据方程式知,C(NaOH)=
| 0.2mol |
| (0.24-0.2)L |
当沉淀最大时,镁离子和铝离子全部转化为Mg(OH)2、Al(OH)3,溶液中的溶质是Na2SO4,
根据硫酸钠的化学式得
| 1 |
| 2 |
| ||
| 0.2L |
故答案为:2.5mol/L;
(3)过氧化钠和水反应生成氧气和氢氧化钠,反应方程式为2Na2O2+2H2O=4NaOH+O2↑,根据方程式知,生成n(NaOH)=
| ||
| 2 |
| ||
| 2 |
铝和氢氧化钠反应生成氢气,反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑,根据方程式知,0.2mol完全溶解需要n(NaOH)=0.2mol<0.4mol,所以氢氧化钠过量,则生成氢气体积=
| 0.2mol |
| 2 |
所以生成气体体积=1.12L+6.72L=7.84L,
故答案为:7.84L.
点评:本题考查了镁铝混合物的有关计算,根据图象分析,明确图象中各个拐点溶液中的溶质是解本题关键,注意(3)中要进行过量计算,很多同学不进行过量计算而导致错误,难度较大.

练习册系列答案
相关题目
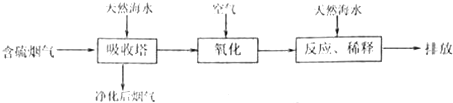
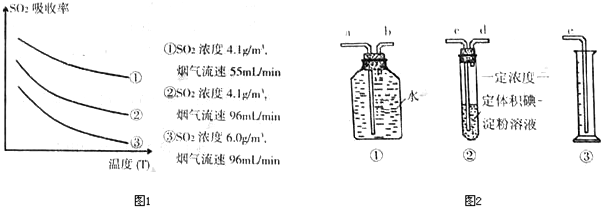
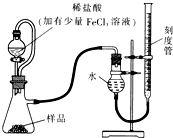 过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.
过氧化镁(MgO2)易溶于稀酸,溶于酸后产生过氧化氢,在医学上可作为解酸剂等.过氧化镁产品中常会混有少量MgO,实验室可通过多种方案测定样品中过氧化镁的含量.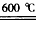 CaCO3
CaCO3 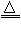 2MgO+C
2MgO+C 
 CH3OH(g)。某研究小组将2 mol
CH3OH(g)。某研究小组将2 mol