题目内容
11.两个容积相同的容器中,一个盛有CO气体,另一个盛有N2气,在同温同压下,两容器内的气体一定具有相同的:①分子数 ②原子数 ③质量 ④密度 ⑤质子数 ⑥电子数( )| A. | 只有①② | B. | 只有①②③ | C. | 只有①②③④ | D. | 全部 |
分析 相同条件下,体积相同的两种容器内气体的物质的量相等,分子数相等,CO、N2都是双原子分子,则含有原子数目一定相等,CO、N2的摩尔质量均为28g/mol,二者质量相等、密度相等,CO分子含有14个质子,而氮分子含有14个质子,则含有质子数目不相等,电子总数等于质子总数.
解答 解:①同温同压下,两个体积相等的容器,一个盛有CO,另一个盛有N2,则CO物质的量等于N2的物质的量,故两容器内含有分子数相等,故①正确;
②CO、N2都是双原子分子,则含有原子数目一定相等,故②正确;
③CO、N2的摩尔质量均为28g/mol,二者物质的量相等,根据m=nM可知,二者质量相等,故③正确;
④同温同压下气体密度之比等于其摩尔质量之比,二者摩尔质量相等,则二者密度相等,故④正确;
⑤CO分子、氮分子均含有14个质子,故二者含有质子数相等,故⑤正确;
⑥电子总数等于质子总数,质子数相等,则含有电子数也相等,故⑥正确,
故选:D.
点评 本题考查阿伏伽德罗定律及其推论,题目难度不大,注意对物质的量计算有关公式理解与灵活应用,注意把握分子的组成.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案
相关题目
1.在一定条件下,将N2和H2按体积比1:3混合充入某密闭容器中,发生反应:N2+3H2?2NH3.当反应在平衡时,恢复到原温度和压强下,测得NH3的体积分数为40%,则N2在平衡混合体系中的体积分数为( )
| A. | 15% | B. | 20% | C. | 30% | D. | 40% |
19.下列四组溶液分别倒入四只烧杯中,并加蒸馏水稀释至50mL,其中NO${\;}_{3}^{-}$物质的量浓度最大的是( )
| A. | 30 mL 1 mol/L的KNO3溶液 | B. | 20 mL 0.5 mol/L的Ba(NO3)2溶液 | ||
| C. | 10 mL 0.6 mol/L的Mg(NO3)2溶液 | D. | 40 mL 0.3 mol/L的Fe(NO3)3溶液 |
6.下列说法中正确的是( )
| A. | S-诱抗素的分子结构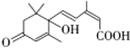 中含有苯环、羟基、羰基、羧基(提示: 中含有苯环、羟基、羰基、羧基(提示: 是羰基) 是羰基) | |
| B. | 1mol阿司匹林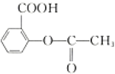 可与2molNaOH发生反应 可与2molNaOH发生反应 | |
| C. | 食品香精菠萝酯的生产路线(反应条件略去)如下图,步骤(2)产物中残留的烯丙醇可用溴水检验: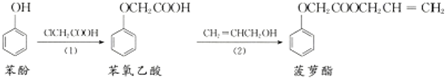 | |
| D. | 有机物A为茉莉香型香料.已知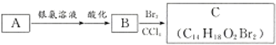 ,则A的分子式为C14H18O ,则A的分子式为C14H18O |
20. 现有A、B、C、D、E五种元素,前四种短周期元素在周期表中的位置如图所示,D的主要化合价为-2、+6,E2+的质子数比D的质子数多4,下列说法正确的是( )
现有A、B、C、D、E五种元素,前四种短周期元素在周期表中的位置如图所示,D的主要化合价为-2、+6,E2+的质子数比D的质子数多4,下列说法正确的是( )
 现有A、B、C、D、E五种元素,前四种短周期元素在周期表中的位置如图所示,D的主要化合价为-2、+6,E2+的质子数比D的质子数多4,下列说法正确的是( )
现有A、B、C、D、E五种元素,前四种短周期元素在周期表中的位置如图所示,D的主要化合价为-2、+6,E2+的质子数比D的质子数多4,下列说法正确的是( )| A. | C可分别与A、E元素形成离子化合物 | |
| B. | D可形成三种价态的酸 | |
| C. | 原子半径:E>D>B>A>C | |
| D. | 最常见气态氢化物的稳定性:C>B>D>A |
 ;试剂加入顺序是先加入浓硝酸,最后加入浓硫酸,该反应需要控制温度,方法是水浴加热.
;试剂加入顺序是先加入浓硝酸,最后加入浓硫酸,该反应需要控制温度,方法是水浴加热.