题目内容
【题目】将0.2molMn02和50mL12mol/L盐酸混合后加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸的挥发)( )
A. 等于0.3mol B. 小于0.3mol C. 大于 0.3mol,小于 0.6mol D. 等于 0.6mol
【答案】C
【解析】
MnO2只与浓盐酸反应生成氯气和氯化锰,随着盐酸浓度的降低,HCl的还原性减弱,反应停止,以此解答该题。
n(MnO2)=0.2mol,n(HCl)=0.05L×12mol/L=0.6mol.反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,根据方程式可知MnO2过量,如盐酸完全反应,则生成0.15molCl2,溶液剩余0.3molCl-,但MnO2只与浓盐酸反应生成氯气和氯化锰,随着盐酸浓度的降低,HCl的还原性减弱,反应停止,所以溶液中剩余Cl-大于0.3mol,小于0.6mol,则反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量大于0.3mol,小于0.6mol。故答案选C。
MnCl2+Cl2↑+2H2O,根据方程式可知MnO2过量,如盐酸完全反应,则生成0.15molCl2,溶液剩余0.3molCl-,但MnO2只与浓盐酸反应生成氯气和氯化锰,随着盐酸浓度的降低,HCl的还原性减弱,反应停止,所以溶液中剩余Cl-大于0.3mol,小于0.6mol,则反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量大于0.3mol,小于0.6mol。故答案选C。

【题目】Fe2O3具有广泛的用途。甲同学阅读有关资料得知:在高温下煅烧FeCO3可以得到Fe2O3。为了进一步验证此结论,他做了如下实验:
实验步骤 | 实验操作 |
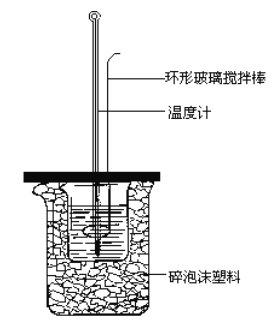
Ⅰ | 取一定质暈的FeCO3固体置于 中,高温煅烧至质量不再减轻,冷却至室溫 |
Ⅱ | 取少量实验步骤Ⅰ所得固体放于一洁净的试管中,用足量的稀硫酸溶解 |
Ⅲ | 向实验步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红 |
由此甲同学得出结论:4FeCO3+O2![]() 2Fe2O3+4CO2
2Fe2O3+4CO2
(1)Ⅰ中横线处所需的化学仪器为______________________________________。
(2)写出实验步骤Ⅲ中发生反应的离子方程式_____________________________。
(3)乙同学提出不同看法:煅烧产物可能是Fe304,因为Fe304也可以溶于硫酸,且所得溶液中也含有Fe3+。于是乙同学对甲同学的实验步骤Ⅲ进行了补充改进:检验实验步骤Ⅱ所得溶液中是否含有Fe2+。他需要选择的试剂是___________________(填序号)。
a.氯水
b.氯水和KSCN溶液
c.酸性高锰酸钾溶液
(4)丙同学认为即使得到了乙同学预期的实验现象,也不能确定煅烧产物的成分。你认为丙同学持此看法的理由是______________________________________。
(5)丙同学进一步査阅资料得知,煅烧FeCO3的产物中的确含有+2价铁元素。于是他设计了另一种由FeCO3制取Fe2O3的方法:先向FeCO3中依次加入试剂:稀硫酸、_____________(填名称)和____________(填名称);再___________________(填操作名称),灼烧,即可得到Fe203。