题目内容
铁、锌合金8.5g溶于稀H2SO4中,充分反应后制得0.300gH2,求合金中Fe,Zn的含量分别为多少克。
m (Fe)= 5.60g;m (Zn) =3.25g
先求出合金的平均摩尔质量:因Fe → H2,Zn → H2 ,合金→ H2,
则合金的平均摩尔质量为:8.5 g /(0.300/2)mol= 59.0g/mol,平均分子量为59.0。
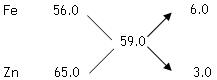
故Fe,Zn分别产生H2的物质的量之比为6.0︰3.0 = 2︰1,从而可知合金中Fe,Zn的质量分别为:
m (Fe)= 56g/mol×(0.300/2)mol×2/3 = 5.60g
m (Zn) = 65g/mol×(0.300/2)mol×1/3 = 3.25g
则合金的平均摩尔质量为:8.5 g /(0.300/2)mol= 59.0g/mol,平均分子量为59.0。

故Fe,Zn分别产生H2的物质的量之比为6.0︰3.0 = 2︰1,从而可知合金中Fe,Zn的质量分别为:
m (Fe)= 56g/mol×(0.300/2)mol×2/3 = 5.60g
m (Zn) = 65g/mol×(0.300/2)mol×1/3 = 3.25g

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
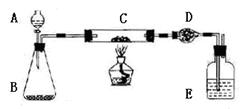






 (1)铜是不活泼的金属,不会和稀硫酸反应,但在盛有铜和稀硫酸的试管中加入双氧水以后,能够看到铜溶解。请写出该反应的离子方程式 。
(1)铜是不活泼的金属,不会和稀硫酸反应,但在盛有铜和稀硫酸的试管中加入双氧水以后,能够看到铜溶解。请写出该反应的离子方程式 。