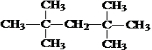题目内容
11.从薄荷油中可得到一种烃A(C10H16),与A相关反应如下: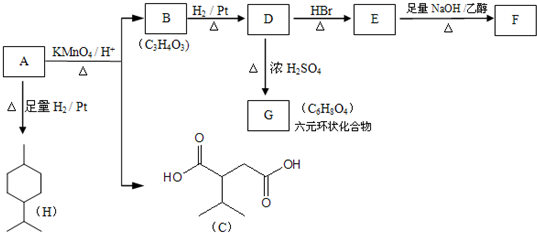
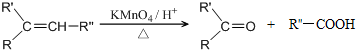
己知:
(1)H的分子式为C10H20.
(2)B→D的反应类型为加成反应.
(3)D既能与乙酸发生酯化反应又能与碳酸钠反应,D中含有的官能团名称为羟基、羧基.
(4)写出由D生成G的化学方程式2
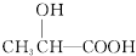 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$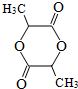 +2H2O.
+2H2O.(5)F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂结构简式为
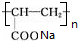 .
.(6)A的一种同分异构体在相同条件下与酸性KMnO4反应也能得到B和C,该有机物的结构简式为
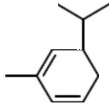 .
.
分析 由A→H的转化加氢,有机物分子的碳链骨架没有变化,可知A分子中含有一个六元环,结合A的分子式C10H16可知还应含有两个不饱和度,再根据题中信息以及C的结构简式、B的分子式可推出A的结构简式为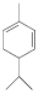 ,则B的结构简式为
,则B的结构简式为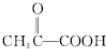 ,B→D加氢,属于加成反应,D既能与乙酸发生酯化反应又能与碳酸钠反应,则D为乳酸
,B→D加氢,属于加成反应,D既能与乙酸发生酯化反应又能与碳酸钠反应,则D为乳酸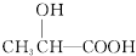 ,由E→F的条件“氢氧化钠的醇溶液加热”,应为卤代烃的消去,逆推可知D→E发生取代反应,溴原子取代了乳酸分子中的羟基,则E、F的结构简式分别为
,由E→F的条件“氢氧化钠的醇溶液加热”,应为卤代烃的消去,逆推可知D→E发生取代反应,溴原子取代了乳酸分子中的羟基,则E、F的结构简式分别为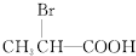 和
和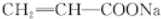 ,G为两个D发生分子内脱水形成,结构简式为
,G为两个D发生分子内脱水形成,结构简式为 ,据此答题.
,据此答题.
解答 解:由A→H的转化加氢,有机物分子的碳链骨架没有变化,可知A分子中含有一个六元环,结合A的分子式C10H16可知还应含有两个不饱和度,再根据题中信息以及C的结构简式、B的分子式可推出A的结构简式为 ,则B的结构简式为
,则B的结构简式为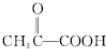 ,B→D加氢,属于加成反应,D既能与乙酸发生酯化反应又能与碳酸钠反应,则D为乳酸
,B→D加氢,属于加成反应,D既能与乙酸发生酯化反应又能与碳酸钠反应,则D为乳酸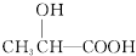 ,由E→F的条件“氢氧化钠的醇溶液加热”,应为卤代烃的消去,逆推可知D→E发生取代反应,溴原子取代了乳酸分子中的羟基,则E、F的结构简式分别为
,由E→F的条件“氢氧化钠的醇溶液加热”,应为卤代烃的消去,逆推可知D→E发生取代反应,溴原子取代了乳酸分子中的羟基,则E、F的结构简式分别为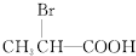 和
和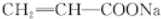 ,G为两个D发生分子内脱水形成,结构简式为
,G为两个D发生分子内脱水形成,结构简式为 ,
,
(1)根据H的结构简式可得分子式为C10H20,故答案为:C10H20;
(2)B→D为羰基与氢气发生的加成反应,故答案为:加成反应;
(3)D为乳酸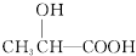 ,D所含官能团的名称为羟基、羧基,故答案为:羟基、羧基;
,D所含官能团的名称为羟基、羧基,故答案为:羟基、羧基;
(4)由D生成G的化学方程式为2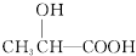 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +2H2O,
+2H2O,
故答案为:2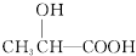 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +2H2O;
+2H2O;
(5)F的结构简式为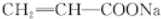 ,F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂结构简式为
,F在一定条件下发生聚合反应可得到一种高吸水性树脂,该树脂结构简式为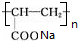 ,
,
故答案为: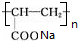 ;
;
(6)A的结构简式为 ,A的一种同分异构体在相同条件下与酸性KMnO4反应也能得到B和C,则该有机物的结构简式为
,A的一种同分异构体在相同条件下与酸性KMnO4反应也能得到B和C,则该有机物的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机合成的分析和推断,注意把握常见有机物的官能团的性质,注意反应条件,比较反应物和生成物的结构确定反应是解答关键,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | 要证明硫酸亚铁铵晶体中含有NH4+,可以取少量晶体溶于水,加入足量NaOH浓溶液并加热,再用湿润的蓝色石蕊试纸检验产生的气体 | |
| B. | KClO3、KNO3、KMnO4等强氧化剂或其混合物不能研磨,否则将引起爆炸 | |
| C. | 常温下用pH试纸分别测定0.1mol•L-1NaClO溶液和0.01mol•L-1NaClO溶液的pH,可以比较浓度对水解程度的影响 | |
| D. | 过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法 |
| a | |||||||
| d | f | g | |||||
| b | c | e | h | ||||
(1)g与b可形成离子化合物b2g,试写出它的电子式
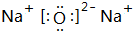 .
.(2)e、f、g 三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示)SiH4<NH3<H2O.
(3)在1L的密闭容器中,通入1mol f2气体和3mol a2气体,一定温度下反应生成fa3气体,2min时,测得f2的浓度为0.75mol•L-1,则2min时fa3的物质的量为0.5mol,a2的化学反应速率v(a2)=0.375 mol•(L•min)-1.
(4)a、d两种元素可形成多种化合物,其中化合物X是最简单的有机物,已知常温下4g X在O2中完全燃烧放出222.4KJ的热量,试写出化合物X完全燃烧的热化学方程式:CH4(g)+2O2(g)→CO2(g)+2H2O(1)H=-889.6kJ/mol.
(5)航天技术中常使用a和g单质组成的碱性燃料电池,该电池具有高能、轻便和不污染环境等优点.该电池正极电极反应式为O2+2H2O+4e-=4OH-.
| A. | 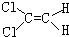 | B. | 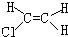 | C. | 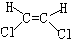 | D. | 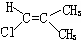 |

| A. | 如图所示的化学反应为放热反应 | |
| B. | 化学反应中有物质变化也有能量变化 | |
| C. | 需要加热的化学反应不一定是吸热反应 | |
| D. | 断裂化学键消耗能量,形成化学键放出能量 |
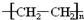 ③
③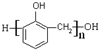 ④油脂 ⑤葡萄糖,请将相应的序号填入空格内.
④油脂 ⑤葡萄糖,请将相应的序号填入空格内.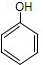 (填结构简式).
(填结构简式).