题目内容
【题目】Ⅰ.常温下,将除去表面氧化膜的Al、Cu片放入U形管作原电池的两极,测得图1所示原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
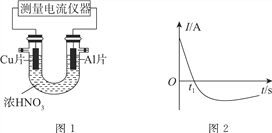
(1)0~t1时,原电池的负极是Al片,此时,正极的电极反应式是________。溶液中的H+向________(填“正”或“负”)极移动。
(2)t1时,原电池中电子流动方向发生改变,其原因是________。
Ⅱ.下图所示电化学装置中,a为足量的电解质溶液,X、Y是两块电极板。
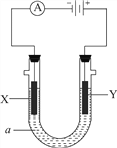
请回答:
(3)若X、Y都是石墨电极,a是含有酚酞的饱和NaCl溶液,则在X电极附近观察到的现象是________,检验Y电极上反应产物的化学方法及实验现象是________,电解池总反应的离子方程式为________。
【答案】 2H++NO3-+e-=NO2↑+H2O 正 Al在浓HNO3中发生钝化,形成的氧化膜阻止了Al的进一步反应 X电极上放出无色气体,附近溶液变为红色 把湿润的碘化钾淀粉试纸放在Y电极附近的U形管出口处,试纸变为蓝色 2C1-+2H2O![]() 2OH+H2↑+Cl2↑
2OH+H2↑+Cl2↑
【解析】(1)0~t1时,原电池的负极是Al片,溶液中产生红棕色气体是二氧化氮,故正极反应方程式为:2H++NO3-+e-=NO2↑+H2O,此时溶液中的氢离子移向正极;
(2)一段时间后,由于Al与浓硝酸发生钝化,导致原电池中Al作正极,Cu作负极,原电池中电子流动方向发生改变;
(3)X电极上氢离子放电,电极反应式为2H++2e-=H2↑,同时电极附近生成氢氧根离子,导致溶液碱性增强,溶液呈红色;Y电极上氯离子失电子发生氧化反应而生成氯气,氯气具有强氧化性,能将碘离子氧化为碘单质,碘遇淀粉试液变蓝色,所以可以用湿润的碘化钾淀粉试纸放在Y电极附近检验氯气,试纸变蓝色,电极反应式为2Cl--2e-=Cl2↑,电解一段时间之后溶液的PH将会升高,电池反应式为 2C1-+2H2O![]() 2OH+H2↑+Cl2↑。
2OH+H2↑+Cl2↑。

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案【题目】下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ③ | |||||
三 | ⑥ | ④ | ⑤ | ⑦ | ⑩ | ⑧ | ⑨ |
⑴在这10种元素中,非金属性最强的元素是_____ (填“元素符号”);金属性最强的元素是_____(填“元素符号”);化学性质最不活泼的元素是_______(填“元素符号”);元素②简单离子的结构示意图为___________________。
⑵元素①与②中,原子半径较大的是________(填元素符号)。
⑶元素②与⑦的气态氢化物分别为__________和__________ (填化学式),两者的热稳定性大小为:前者_____后者。(填“>”、“<”或“=”)。
⑷元素④与⑧的最高价氧化物的水化物分别为______和______(填“化学式”),
两者反应的离子方程式为__________________________________。
⑸元素⑤的氧化物与盐酸反应的离子方程式为: _______________________。
⑹元素⑧的单质与元素⑩的氢化物反应的化学方程式为:__________________。