题目内容
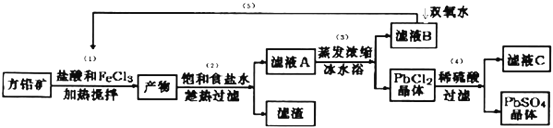
【题目】硫酸铅可用于铅蓄电池、纤维增重剂、涂料分析试剂.工业上通常用自然界分布最广的方铅矿(主要成分为PbS)生产硫酸铅。工艺流程如下:
已知:①Ksp(PbSO4)=1.08×10-8,Ksp(PbCl2)=1.6×l0-5.
②PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0
PbCl42-(aq) △H>0
③Fe3+、Pb2+以氢氧化物形式开始沉淀时的pH值分别为1.9和7.
(I)流程中加入盐酸可以控制溶液的pH<1.9,主要目的是 _____________________,反应过程中可观察到淡黄色沉淀,则步骤(1)对应的主要反应的离子方程式为 ____________________________;
(II)步骤(2)所得的滤液A 蒸发浓缩后再用冰水浴的目的是___________(请用平衡移动原理解释)
(III)上述流程中可循环利用的物质有___________;
(Ⅵ)步骤(4)中反应的离子方程式为_____________________.对滤液C中氯离子的测定可中和后采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl,利用Ag+与CrO42-生成砖红色沉淀,指示到达滴定终点。选用K2CrO4溶液的最好浓度等于 _____________mol·L1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
(Ⅴ)PbO2与MnO2性质相似,请写出PbO2与浓盐酸加热条件下反应的离子方程式______________________
【答案】 抑制Fe3+的水解 2Fe3++PbS+2Cl-=PbCl2+S+2Fe2+ 用冰水浴使PbCl2(s)+2Cl-(aq) ![]() PbCl4-△H>0逆向移动,使PbCl4-转化PbCl2析出 FeCl3、HCl PbCl2+SO42-= PbSO4+2Cl- 5×10-3 PbO2+4H++2Cl-=Pb2++Cl2+2H2O
PbCl4-△H>0逆向移动,使PbCl4-转化PbCl2析出 FeCl3、HCl PbCl2+SO42-= PbSO4+2Cl- 5×10-3 PbO2+4H++2Cl-=Pb2++Cl2+2H2O
【解析】往方铅矿中加入FeCl3溶液和盐酸,FeCl3与PbS反应生成PbCl2和S,产物中加入饱和食盐水,趁热过滤,有利于PbCl2(s)+2Cl-(aq)![]() PbCl4-△H>0正向进行,使PbCl2溶解,过滤除去硫等杂质,滤液A含有PbCl4-、Cl-、Fe2+、Fe3+等,滤液A蒸发浓缩,冷水浴中冷却,利用平衡逆向进行,析出PbCl2晶体,滤液B中含有Fe2+、Fe3+,用过氧化氢进行氧化后循环利用,PbCl2晶体中加入稀硫酸,转化为更难溶的硫酸铅沉淀,过滤得到硫酸铅沉淀,洗涤、烘干得到硫酸铅粉末,滤液C中含有HCl。
PbCl4-△H>0正向进行,使PbCl2溶解,过滤除去硫等杂质,滤液A含有PbCl4-、Cl-、Fe2+、Fe3+等,滤液A蒸发浓缩,冷水浴中冷却,利用平衡逆向进行,析出PbCl2晶体,滤液B中含有Fe2+、Fe3+,用过氧化氢进行氧化后循环利用,PbCl2晶体中加入稀硫酸,转化为更难溶的硫酸铅沉淀,过滤得到硫酸铅沉淀,洗涤、烘干得到硫酸铅粉末,滤液C中含有HCl。
(Ⅰ)Fe3+、Pb2+以氢氧化物形式开始沉淀时的pH值分别为1.9和7,流程中加入盐酸可以控制溶液的pH<1.9,主要目的是:抑制Fe3+的水解,FeCl3与PbS反应生成PbCl2和S,Pb元素化合价不变,S元素化合价升高,则铁元素的化合价降低,有FeCl2生成,反应方程式为:2FeCl3+PbS=PbCl2+S+2FeCl2,反应离子方程式为:2Fe3++PbS=PbCl2+S+2Fe2+;(Ⅱ)用冰水浴使PbCl2(s)+2Cl-(aq)![]() PbCl4-△H>0逆向移动,使PbCl4-转化PbCl2析出;(Ⅲ)过氧化氢将滤液B中Fe2+氧化为Fe3+,再循环利用,C溶液中含有HCl,也可以循环利用;(Ⅳ)①根据以上分析可知步骤(4)中反应的离子方程式为PbCl2+SO42-=PbSO4+2Cl-;当氯离子浓度小于10-5mol/L时可以认为沉淀完全,此时银离子浓度是2.0×10-10/10-5mol/L=2×10-5mol/L,所以铬酸钾的浓度是
PbCl4-△H>0逆向移动,使PbCl4-转化PbCl2析出;(Ⅲ)过氧化氢将滤液B中Fe2+氧化为Fe3+,再循环利用,C溶液中含有HCl,也可以循环利用;(Ⅳ)①根据以上分析可知步骤(4)中反应的离子方程式为PbCl2+SO42-=PbSO4+2Cl-;当氯离子浓度小于10-5mol/L时可以认为沉淀完全,此时银离子浓度是2.0×10-10/10-5mol/L=2×10-5mol/L,所以铬酸钾的浓度是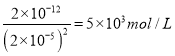 ;(Ⅴ)PbO2与MnO2性质相似,PbO2与浓盐酸加热条件下生成氯气的离子方程式为PbO2+4H++2Cl-
;(Ⅴ)PbO2与MnO2性质相似,PbO2与浓盐酸加热条件下生成氯气的离子方程式为PbO2+4H++2Cl-![]() Pb2++Cl2+2H2O。
Pb2++Cl2+2H2O。

【题目】在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22:9,当1.6克X与Y完全反应后,生成4.4克R,则在此反应中Y和M的质量之比为( )
A.16:9
B.23:9
C.32:9
D.46:9
【题目】下表中物质的分类组合完全正确的是( )
编组 | A | B | C | D |
强电解质 | NaCl | H2SO4 | CaCO3 | H2S |
弱电解质 | HF | BaSO4 | HClO | NH3·H2O |
非电解质 | Cl2 | CS2 | CH4 | 蔗糖 |
A. AB. BC. CD. D