题目内容
【题目】据《天工开物》记载,我国古代以炉甘石(主要成分是ZnCO3)来升炼倭铅(即锌),其原理如图。已知锌的熔点420 ℃、沸点906 ℃。则下列说法不正确的是
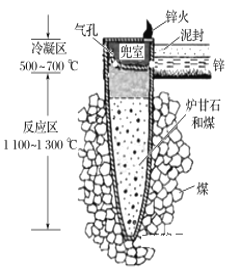
A. 升炼倭铅过程包含分解反应和氧化还原反应
B. 冶炼时锌变为蒸气在兜室冷凝为固体
C. “泥封”的目的是为了防止得到的锌被氧化
D. “锌火”是锌蒸气和一氧化碳在空气的燃烧
【答案】B
【解析】
根据题目提供的图片分析反应流程分析解答;根据氧化还原反应的本质和特征分析解答。
A.“升炼倭铅”的过程中主要反应有:ZnCO3在高温条件下分解生成CO2和ZnO,CO2与C反应生成CO,CO+ZnO![]() Zn(g)+CO2,有分解反应,也有氧化还原反应,故A正确;
Zn(g)+CO2,有分解反应,也有氧化还原反应,故A正确;
B. 反应区温度达到1100~1300℃,Zn变为蒸气与杂质分离,在“兜室”冷凝为液体流出(冷凝区温度高于Zn的熔点、低于其沸点),故B错误;
C.Zn易被空气氧化,为防止Zn被氧化而用“泥封”隔绝空气,故C正确;
D.“锌火”是未反应完的CO和Zn蒸气从“兜室”逸出燃烧,故D正确。
故选B。

【题目】下图为元素周期表的一部分,根据元素a~j在周期表中的位置,按要求回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | a | |||||||
2 | b | c | d | e | ||||
3 | f | g | h | i | j | |||
(1)在a ~j中,化学性质最不活泼的元素是___________(填元素符号)。
(2)f、g、h的单质分别与水反应,最剧烈的是___________(填元素符号)。
(3)c、i的氢化物稳定性较强的是____________(填化学式)。
(4)c、f可形成既含离子键又含非极性键的化合物,该化合物的电子式为__________。
(5)d、f、g的离子半径最大的是_______________(填离子符号)。
(6)f的最高价氧化物的水化物与h的最高价氧化物的水化物反应的离子方程式为:___________________________________。