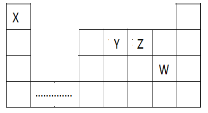
题目内容
【题目】下列示意图与对应的反应情况符合的是
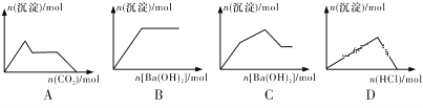
A. 向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量
B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
C. 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量
D. 向NaAlO2溶液中逐滴加入盐酸至过量
【答案】B
【解析】
试题A选项首先CO2先与Ca(OH)2反应,产生CaCO3沉淀,此时沉淀量保持不变,CO2再和KOH反应,此时无沉淀,之后二氧化碳先会和K2CO3反应,生成酸式盐,当反应完全之后再和沉淀CaCO3反应,生成碳酸氢钙,从而沉淀出现溶解现象,所以图像应该是“等腰梯形”的形状,故A错误;B选项,假设溶液中含1 mol KAl(SO4)2,加入1.5 mol的Ba(OH)2时生成1.5mol BaSO4和1 mol Al(OH)3,沉淀的物质的量最大为2.5 mol,再加入0.5 mol Ba(OH)2,生成0.5 mol BaSO4,溶解1 mol Al(OH)3,故沉淀的总物质的量减少,但产生沉淀的过程不会出现折点,最后只剩下硫酸钡沉淀,故B错误;C选项NaHSO4溶液中逐滴加入Ba(OH)2溶液,只产生硫酸钡沉淀,当把硫酸根反应完全,再加氢氧化钡也不产生沉淀,所给图像恰好能表达该反应过程,故C选项正确。D选项NaAlO2溶液中逐滴加入稀盐酸,在NaAlO2与HCl的物质的量之比为小于等于1︰1, 此时只生成白色的氢氧化铝沉淀,如果继续加入盐酸,这是沉淀开始溶剂,当NaAlO2与HCl的物质的量之比达到1︰4时,所产生的氢氧化铝完全溶解,离子方程式如下,H++AlO2-+ H2O = Al(OH)3↓; Al(OH)3+3H+ = Al3+ + 3H2O故曲线应该是加入1份盐酸时沉淀达到最大,再加入3份盐酸沉底全部消失,图像应该是个“非等腰三角形”,与D所给图像不符合,故D错误。
考点:常见反应过程与现象 化学图像

 科学实验活动册系列答案
科学实验活动册系列答案【题目】研究弱电解质的电离,有重要的实际意义。
Ⅰ. 醋酸是一种常见的有机酸。
(1)醋酸的电离方程式为__________________________________________________。
(2)保持温度不变,向醋酸溶液中通入一定量的氨气,下列量将变小的是________。
A. c(CH3COO-) B. c(H+)
C. c(OH-) D. CH3COOH电离平衡常数
(3)向0.1 mol·L-1 CH3COOH溶液中加水稀释,c(CH3COO-) / c(CH3COOH)的比值将________(填“变大”、“不变”或“变小”)。
(4)下列事实一定能说明CH3COOH是弱电解质的是____________(填字母)。
A. 相同温度下,浓度均为1 mol·L-1的盐酸和醋酸的导电性对比:盐酸>醋酸
B. 1 mol·L-1 CH3COOH溶液能使紫色石蕊试液变红
C. 25℃时,1 mol·L-1 CH3COOH溶液的pH约为2
D. 10 mL 1mol·L-1的CH3COOH溶液恰好与10 mL 1mol·L-1 NaOH溶液完全反应
Ⅱ. 对比酸性的相对强弱
(5)现有a. CH3COOH b. HCl两种溶液,请回答下列问题(填“>”、“<”或“=”)。
① 将pH相同的两种酸溶液分别稀释100倍后,pH的大小关系为a_______b。
② pH相同、体积相同的两种酸溶液中分别加入足量锌,相同状况下产生气体体积大小关系为a_______b。
③ 将体积相同、pH=2的醋酸和pH=2的盐酸分别与pH=12的氢氧化钠溶液等体积混合,反应后溶液的pH的大小关系为a_______b。
④ 相同物质的量浓度的两种酸溶液中,水的电离程度的大小关系为a_______b。
(6)某些弱酸的电离常数如下:
化学式 | CH3COOH | HSCN | HCN | HClO | H2CO3 |
电 离 常 数 | 1.8×10-5 | 1.3×10-1 | 4.9×10-10 | 3.0×10-8 | K1=4.4×10-7 K2=4.7×10-11 |
①下列反应可以发生的是__________(填字母)。
A. CH3COOH+Na2CO3=NaHCO3+CH3COONa
B. CH3COOH+NaCN=CH3COONa+HCN
C. CO2+H2O+2NaClO=Na2CO3+2HClO
D. NaHCO3+HCN=NaCN+H2O+CO2↑
②25℃时,将20 mL 1 mol·L-1 CH3COOH溶液和20 mL 1 mol·L-1 HSCN溶液分别与20 mL1 mol·L-1 NaHCO3溶液混合,画出产生的CO2气体体积(V)随时间(t)的变化关系图,并注明对应酸的化学式。__________
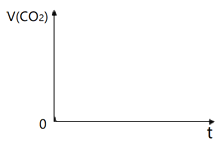 。
。
【题目】2 L密闭容器中进行反应:pZ(g)+qQ(g) ![]() mX(g)+nY(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
mX(g)+nY(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
物质 | X | Y | Z | Q |
起始/mol | 0.7 | 1 | ||
2 min末/mol | 0.8 | 2.7 | 0.8 | 2.7 |
3 min末/mol | 0.8 |
已知:2 min内v(Q)=0.075 mol·L-1·min-1,v(Z)∶v(Y)=1∶2。
请回答下列问题:
(1)2 min内X的反应速率v(X)=__________。
(2)起始时n(Y)=__________。
(3) 3 min末是否达到平衡_______(填是或否)。
(4)对于该反应,能增大正反应速率的措施是________(填序号,下同)。
A.缩小容器体积 B.移走部分Q
C.通入大量He气 D.升高温度