题目内容
20.在某一密闭容器中,若反应2NO2(g)?N2O4(g)达到平衡后,保持其温度不变,将该密闭容器的体积增加一倍,当达到新的平衡时,则下列说法正确的是( )| A. | 容器内气体密度减小 | B. | 平衡向正反应方向移动 | ||
| C. | 二氧化氮的转化率增大 | D. | 四氧化二氮的体积分数减小 |
分析 在某一密闭容器中,若反应2NO2(g)?N2O4(g)达到平衡后,保持其温度不变,将该密闭容器的体积增加一倍,压强减小,平衡逆向进行,气体物质的量增大.
解答 解:在某一密闭容器中,若反应2NO2(g)?N2O4(g)达到平衡后,保持其温度不变,将该密闭容器的体积增加一倍,压强减小,平衡逆向进行,气体物质的量增大,
A、平衡状态气体质量不变,气体体积增大,密度减小,故A正确;
B、上述分析可知平衡逆向进行,故B错误;
C、平衡逆向进行,二氧化氮转化率减小,故C错误;
D、平衡逆向进行,四氧化二氮的体积分数减小,故D正确;
故选AD.
点评 本题考查了化学平衡的影响因素分析判断,主要是化学平衡移动原理的实质理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
4.在一定条件下,下列微粒的还原性顺序为Cl-<Br-<Fe2+<I-<SO2,由此判断以下各反应在溶液中不能发生的是( )
| A. | 2Br-+4H++SO${\;}_{4}^{2-}$═SO2+Br2+2H2O | |
| B. | 2Fe3++SO2+2H2O═2Fe2++SO${\;}_{4}^{2-}$+4H+ | |
| C. | 2Fe2++Cl2═2Fe3++2Cl- | |
| D. | I2+SO2+2H2O═4H++SO${\;}_{4}^{2-}$+2I- |
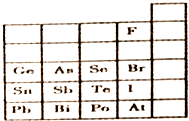
11.下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:Ar(填具体元素符号或化学式,下同),非金属性最强的元素是:F.
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:HClO4,碱性最强的化合物的化学式是:KOH.
(3)最高价氧化物是两性氧化物的元素是:Al;写出它的最高价氧化物与氢氧化钠反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).
,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:HClO4,碱性最强的化合物的化学式是:KOH.
(3)最高价氧化物是两性氧化物的元素是:Al;写出它的最高价氧化物与氢氧化钠反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O.
(4)④与⑧形成的化合物的电子式是:
 ,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).
,该化合物所含化学键类型是:离子键(填“共价键”或“离子键”).(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 实验步骤 | 实验现象与结论 |
| . |
5.下列物质属于弱电解质的( )
| A. | 氨水 | B. | 水 | C. | 硫酸钡 | D. | 酒精 |
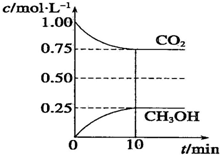 在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ.mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.
在一定温度下的2L固定容积的密闭容器中,通入2mol CO2和3mol H2,发生的反应为CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-akJ.mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示.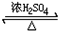 CH3COOC2H5+H2O;④2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;⑤CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O.
CH3COOC2H5+H2O;④2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;⑤CH3CH2Br+NaOH$→_{△}^{醇}$CH2=CH2↑+NaBr+H2O.