��Ŀ����
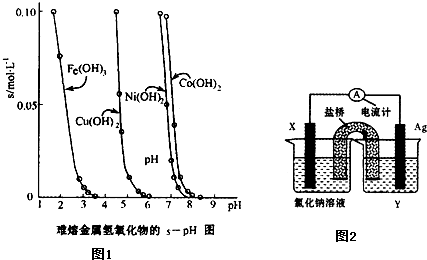
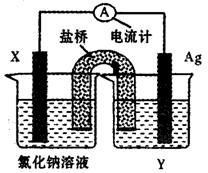
 �������������������ܽ�Ȳ�ͬ����˿���������һ���ʣ�������Һ��pH���ﵽ����������ӵ�Ŀ�ģ����ܽ��������������ڲ�ͬpH�µ��ܽ�ȣ�s��mol?L-1����ͼ��
�������������������ܽ�Ȳ�ͬ����˿���������һ���ʣ�������Һ��pH���ﵽ����������ӵ�Ŀ�ģ����ܽ��������������ڲ�ͬpH�µ��ܽ�ȣ�s��mol?L-1����ͼ����1��pH=3ʱ��Һ��ͭԪ�ص���Ҫ������ʽ�ǣ�
Cu2+
Cu2+
����д��ѧʽ����2����Ҫ��ȥCuCl2��Һ�е�����Fe3+��Ӧ�ÿ�����Һ��pHΪ
B
B
��������ĸ��A����1 B��4���� C����6
��3����Ni��NO3��2��Һ�к���������Co2+���ʣ�
����
����
���ܡ����ܣ�ͨ��������ҺpH�ķ�������ȥ��������Co2+��Ni2+������pH��Χ���̫С
Co2+��Ni2+������pH��Χ���̫С
����4��Ҫʹ������ͭ�����ܽ⣬���˼�����֮�⣬�����Լ��백ˮ������[Cu��NH3��4]2+��д����Ӧ�����ӷ���ʽ��
Cu��OH��2+4NH3?H2O=[Cu��NH3��4]2++2OH-+4H2O
Cu��OH��2+4NH3?H2O=[Cu��NH3��4]2++2OH-+4H2O
����5����֪һЩ��������ܶȻ��������±���
| ���� | FeS | MnS | CuS | PbS | HgS | ZnS |
| Ksp | 6.3��10-18 | 2.5��10-13 | 1.3��10-36 | 3.4��10-28 | 6.4��10-53 | 1.6��10-24 |
B
B
��ȥ���ǣ�A��NaOH �������� B��FeS �������� C��Na2S������������ѡ����ţ�
��������1����pH=3ʱ����Һ�в������Cu��OH��2������
��2����ȥFe3+��ͬʱ���뱣֤Cu2+���ܳ��������pHӦ������4���ң�
��3��Co2+��Ni2+������pH��Χ���̫С��
��4�����ݷ�Ӧ����������д����Ӧ�ķ���ʽ��
��5��Ҫʹ�����������ɳ��������ѡ��������ˮ��FeS��ʹ����ת��Ϊ�����ܽ�Ľ������������ͬʱ�ֲ������������ӣ�
��2����ȥFe3+��ͬʱ���뱣֤Cu2+���ܳ��������pHӦ������4���ң�
��3��Co2+��Ni2+������pH��Χ���̫С��
��4�����ݷ�Ӧ����������д����Ӧ�ķ���ʽ��
��5��Ҫʹ�����������ɳ��������ѡ��������ˮ��FeS��ʹ����ת��Ϊ�����ܽ�Ľ������������ͬʱ�ֲ������������ӣ�
����⣺��1����ͼ��֪����pH=3ʱ����Һ�в������Cu��OH��2��������Ҫ��Cu2+���ڣ��ʴ�Ϊ��Cu2+��
��2����ȥFe3+��ͬʱ���뱣֤Cu2+���ܳ��������pHӦ������4����Fe3+������ȫ���ʴ�Ϊ��B��
��3����ͼʾ��ϵ�ɿ�����Co2+��Ni2+������pH��Χ���̫С����������Һ��pH��
�ʴ�Ϊ�����ܣ�Co2+��Ni2+������pH��Χ���̫С��
��4��������ͭ�������ڰ�ˮ����=[Cu��NH3��4]2+����Ӧ�����ӷ���ʽΪCu��OH��2+4NH3?H2O=[Cu��NH3��4]2++2OH-+4H2O��
�ʴ�Ϊ��Cu��OH��2+4NH3?H2O=[Cu��NH3��4]2++2OH-+4H2O��
��5��Ҫʹ�����������ɳ��������ѡ��������ˮ��FeS��ʹ����ת��Ϊ�����ܽ�Ľ������������ͬʱ�ֲ������������ӣ��ʴ�Ϊ��B��
��2����ȥFe3+��ͬʱ���뱣֤Cu2+���ܳ��������pHӦ������4����Fe3+������ȫ���ʴ�Ϊ��B��
��3����ͼʾ��ϵ�ɿ�����Co2+��Ni2+������pH��Χ���̫С����������Һ��pH��
�ʴ�Ϊ�����ܣ�Co2+��Ni2+������pH��Χ���̫С��
��4��������ͭ�������ڰ�ˮ����=[Cu��NH3��4]2+����Ӧ�����ӷ���ʽΪCu��OH��2+4NH3?H2O=[Cu��NH3��4]2++2OH-+4H2O��
�ʴ�Ϊ��Cu��OH��2+4NH3?H2O=[Cu��NH3��4]2++2OH-+4H2O��
��5��Ҫʹ�����������ɳ��������ѡ��������ˮ��FeS��ʹ����ת��Ϊ�����ܽ�Ľ������������ͬʱ�ֲ������������ӣ��ʴ�Ϊ��B��
���������⿼���˳����ܽ�ƽ�⼰����ˮ���Ӧ���Լ��ܶȻ��ļ��㣬��Ŀ�Ѷ��еȣ������Ĺؼ����������⣬�ܴ�ͼ�����ߵı仯�ص�������ʵ��ܽ��ԣ�

��ϰ��ϵ�д�
 ����ѧ��Ӧ�����ϵ�д�
����ѧ��Ӧ�����ϵ�д�
�����Ŀ
(10��)�������������������ܽ�Ȳ�ͬ����˿���������һ���ʣ�������Һ��pH���ﵽ����������ӵ�Ŀ�ġ����ܽ��������������ڲ�ͬpH�µ��ܽ��(s��mol��L��1)����ͼ��
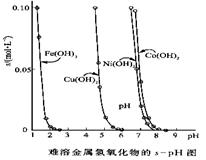
(1)pH��3ʱ��Һ��ͭԪ�ص���Ҫ������ʽ�ǣ�________(��ѧʽ)
(2)��Ҫ��ȥCuCl2��Һ�е�����Fe3����Ӧ�ÿ�����Һ��pHΪ
A����1 B��4���� C����6
(3)��Ni(NO3)2��Һ�к���������Co2�����ʣ�___ (�ܡ�����)ͨ��������ҺpH�ķ�������ȥ��������_________��
(4)��֪һЩ��������ܶȻ��������±���
|
���� |
FeS |
MnS |
CuS |
PbS |
HgS |
ZnS |
|
Ksp |
6.3��10��18 |
2.5��10��13 |
1.3��10��36 |
3.4��10��28 |
6.4��10��53 |
1.6��10��24 |
ij��ҵ��ˮ�к���Cu2����Pb2����Hg2������������˹�ҵ��ˮ�м��������_______��ȥ���ǡ�
A��NaOH B��FeS C��Na2S
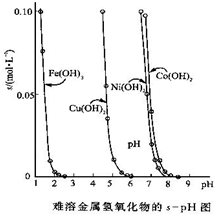 �������������������ܽ�Ȳ�ͬ����˿���������һ���ʣ�������Һ��pH���ﵽ����������ӵ�Ŀ�ģ����ܽ��������������ڲ�ͬpH�µ��ܽ�ȣ�s��mol?L-1����ͼ��
�������������������ܽ�Ȳ�ͬ����˿���������һ���ʣ�������Һ��pH���ﵽ����������ӵ�Ŀ�ģ����ܽ��������������ڲ�ͬpH�µ��ܽ�ȣ�s��mol?L-1����ͼ��