题目内容
下列说法正确的是( )A.二氧化碳通入硅酸钠溶液中可以得到硅酸
B.二氧化硅是酸性氧化物,它可以跟强碱反应而不跟任何酸反应
C.二氧化硅对应的水化物有不同的组成,如H4SiO4叫原硅酸,H2SiO3叫硅酸
D.根据SiO2+CaCO3![]() CaSiO3+CO2↑的反应,可推知硅酸的酸性比碳酸强
CaSiO3+CO2↑的反应,可推知硅酸的酸性比碳酸强
解析:A项的说法正确,其反应的化学方程式:NaSiO3+CO2+H2O=Na2CO3+H2SiO3↓,SiO2与绝大多数酸不反应,但可以与氢氟酸反应:SiO2+4HF=SiF4↑+2H2O(工业上用此反应雕刻玻璃),因此,B选项中所提SiO2不与任何酸反应的说法是不正确的;C项的说法正确,原硅酸不稳定,易失去水分变成硅酸H4SiO4=H2SiO3+H2O;D项中SiO2和CaCO3的反应说明,高温下,难挥发性酸酐(SiO2)可制出挥发性酸酐(CO2),但不能说明硅酸酸性比碳酸强,因为物质的酸性强弱比较是指在水溶液的情况下,而不是在高温下。因此本题选A、C。
答案:AC

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目

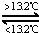 Sn(s,白)△H3=+2.1kJ?mol-1,
Sn(s,白)△H3=+2.1kJ?mol-1,