题目内容
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化碳(![]() )排放量减少8%,氮氧化物(
)排放量减少8%,氮氧化物(![]() )排放量减少10%。目前,消除大气污染有多种方法,利用钠碱循环法可脱除烟气中的
)排放量减少10%。目前,消除大气污染有多种方法,利用钠碱循环法可脱除烟气中的![]() 。
。
(1)在钠碱循环法中, ![]() 溶液作为吸收液,可由NaOH溶液吸收
溶液作为吸收液,可由NaOH溶液吸收![]() 制得,该反应的离子方程式是_______________________。
制得,该反应的离子方程式是_______________________。
(2)吸收液吸收![]() 的过程中,pH随
的过程中,pH随![]() 变化关系如下表:
变化关系如下表:
| 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断![]() 溶液显______________性,用化学平衡原理解释:_____________。
溶液显______________性,用化学平衡原理解释:_____________。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):___________。
a. ![]()
b. ![]()
c. ![]()
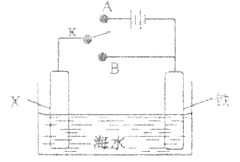
(3)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
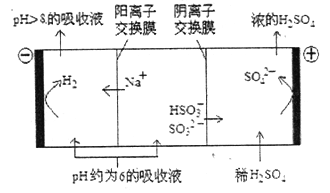
①![]() 在阳极放电的电极反应式是________________。
在阳极放电的电极反应式是________________。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理:
_________________。
【答案】 ![]() 酸性
酸性 ![]() 中存在:
中存在: ![]()
![]()
![]()
![]()
![]() ,
, ![]() 电离程度大于其水解程度 a b
电离程度大于其水解程度 a b ![]()
![]() 在阴极得电子生成
在阴极得电子生成![]() ,溶液中的
,溶液中的![]() 降低,促使
降低,促使![]() 电离生成
电离生成![]() ,且
,且![]() 进入阴极室,吸收液得以再生
进入阴极室,吸收液得以再生
【解析】(1)NaOH溶液吸收![]() 制得
制得![]() 和水,反应的离子方程式为:
和水,反应的离子方程式为: ![]() ;(2)①由表格中的数据可知,
;(2)①由表格中的数据可知, ![]() 越多,酸性越强,则
越多,酸性越强,则![]() 中存在:
中存在: ![]()
![]()
![]()
![]()
![]() ,
, ![]() 电离程度大于其水解程度;②吸收液呈中性时,溶质为亚硫酸钠和亚硫酸氢钠,电离与水解的程度相等,a.由电荷守恒可知,
电离程度大于其水解程度;②吸收液呈中性时,溶质为亚硫酸钠和亚硫酸氢钠,电离与水解的程度相等,a.由电荷守恒可知, ![]() ,中性溶液则
,中性溶液则![]() ,则
,则![]() ,选项a正确;b.
,选项a正确;b. ![]()
![]()
![]() ,
, ![]()
![]()
![]() ,亚硫酸两步水解,则离子浓度为
,亚硫酸两步水解,则离子浓度为![]() ,选项b正确;c.
,选项b正确;c. ![]() 中不遵循电荷守恒,选项c错误;答案选ab;(3)①当吸收液的pH降至约为6时,吸收液中阴离子主要是亚硫酸氢根离子,亚硫酸氢根离子在阳极上失电子和水反应生成硫酸根离子和氢离子,电极反应式为:
中不遵循电荷守恒,选项c错误;答案选ab;(3)①当吸收液的pH降至约为6时,吸收液中阴离子主要是亚硫酸氢根离子,亚硫酸氢根离子在阳极上失电子和水反应生成硫酸根离子和氢离子,电极反应式为: ![]() ;②电解时,溶液中阳离子向阴极移动,氢离子在阴极得电子生成氢气,溶液中氢离子浓度降低,导致加速
;②电解时,溶液中阳离子向阴极移动,氢离子在阴极得电子生成氢气,溶液中氢离子浓度降低,导致加速![]() 电离生成
电离生成![]() ,钠离子进入阴极室,吸收液就可以再生。
,钠离子进入阴极室,吸收液就可以再生。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】向1.0 mol/L的甲溶液中逐滴加入1.0 mol/L的乙溶液,产生Al(OH)3沉淀的质量(用y轴表示)与所加入乙溶液的体积(用x轴表示)的关系如下图所示,符合图中关系的是下列各组溶液中的( )
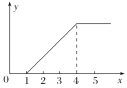
A | B | C | D | |
甲 | AlCl3 | NaOH | NaAlO2 | HCl |
乙 | NaOH | AlCl3 | HCl | NaAlO2 |
A. A B. B C. C D. D