��Ŀ����
����Ŀ����ѧ����������������ء��밴Ҫ�ش��������⣺
(1)���˽����������������α������������Ƴɣ�������ijɷֿɼ����� Ca2Mg5Si8O22(OH)2�����������������ʽ�ɱ�ʾΪ___________________��
(2)�й�Na2CO3��NaHCO3 ����;������������ͷ۵���Ҫ�ɷ�֮һ�ǣ�д�׳ƣ�________��д�����������У�������������θ������ҩ����θ�ᷴӦ�����ӷ���ʽ____________��
(3)��Ư�������ڱ�¶�ڿ����л���ʣ�������Ϊ��Ư����������ж�����̼�Ӵ����Ӷ�ʧȥ��Ư���ԡ�д���ò���Ӧ�Ļ�ѧ��Ӧ����ʽ___________________________��
���𰸡�2CaO5MgO8SiO2H2O С�մ� H++HCO3-=H2O+CO2�� Ca(ClO)2+CO2+H2O=CaCO3��+2HclO��2HClO![]() 2HCl+O2��(��дҲ���Բ�д��
2HCl+O2��(��дҲ���Բ�д��
��������
(1)����������SiΪ+4�ۣ�CaΪ+2�ۣ�MgΪ+2�ۣ�HΪ+1�ۣ�OΪ-2�ۣ����ݻ��ϼ��ж������ﻯѧʽ���ݴ���д��
(2) NaHCO3�Ƿ��ͷ۵���Ҫ�ɷ֣����ݶ���ˮ��Һ�ļ���ǿ�����Ƿ�����д̼��Է����жϣ�������д��Ӧ�����ӷ���ʽ��
(3)Ư���ڿ����б�������Ϊ����Ч�ɷ�Ca(ClO)2��������е�CO2��H2O��Ӧ����HClO��HClO�ֽ�ʹƯ�۱���ʧЧ��
(1)���ݹ����θ�д�����������ʽΪ�����ý����������ϻ��ý�����������������ˮ��ͬʱҪ��ѭԭ���غ㣬Ca2Mg5Si8O22(OH)2�ɱ�ʾΪ��2CaO5MgO8SiO2H2O��
(2)NaHCO3�DZ��ո��������ͷ۵���Ҫ�ɷ�֮һ�����׳���С�մ�
Na2CO3��Һ����ǿ�����˻����ǿ�ҵĴ̼����ã�������������θ����࣬NaHCO3��Һ��������������θ��(������)��Ӧ�����Ȼ��ơ�ˮ��������̼����˿�����θ����࣬��Ӧ�����ӷ���ʽΪ��H++HCO3-=H2O+CO2����
(3)Ư�۵���Ч�ɷ���Ca(ClO)2���������ڿ����б�������Ϊ����Ч�ɷ�Ca(ClO)2��������е�CO2��H2O��Ӧ����HClO��HClO�ֽ�ʹƯ�۱���ʧЧ����Ӧ�Ļ�ѧ����ʽΪ��Ca(ClO)2+CO2+H2O=CaCO3��+2HClO��2HClO![]() 2HCl+O2����
2HCl+O2����

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ������������������۷���Ϣ�صijɷ�֮һ�������㽶����ζ��ʵ�����Ʊ������������ķ�Ӧ��װ��ʾ��ͼ���й��������£�
��Է������� | �ܶ�/��gcm-3�� | �е�/�� | ˮ���ܽ��� | |
���촼 | 88 | 0.8123 | 131 | �� |
���� | 60 | 1.0492 | 118 | �� |
���������� | 130 | 0.8670 | 142 | ���� |

ʵ�鲽�裺
��A�м���4.4 g���촼(3-��-1-�촼)��6.0 g���ᡢ����Ũ�����2��3Ƭ���Ƭ����ʼ��������A������50 min����ӦҺ�������º����Һ©���У��ֱ�������ˮ������̼��������Һ��ˮϴ�ӣ��ֳ��IJ������������ˮMgSO4���壬����Ƭ�̣����˳�ȥMgSO4���壬�����������ռ�140��143����֣�������������3.9 g��
�ش��������⣺
��1������B�ľ���������____________��ʵ��ʱ��ȴˮ�Ľ�ˮ����_____��a��b����
��2����ϴ�Ӳ����У���ˮϴ�ٱ���NaHCO3��Һϴ������ֱ���ñ���NaHCO3��Һϴ�ӵ�ԭ����____________________��
��3�����Ʊ���Ӧ�Ļ�ѧ��Ӧ����ʽΪ__________________________��
��4����ʵ���м�����������Ŀ����___________________________��
��5����ʵ���в�������ʯ�Ҵ�����ˮMgSO4��ԭ��________________________��
��6������������У�����ѡ��װ����ȷ����___________(����)��

��7����ʵ��IJ�����___________(����)��
a.90% b.60% c.40% d.30%
����Ŀ��ijǿ������ɫ��Һ�п��ܺ��±��е����������ӡ�
������ | Mg2+��NH4+��Ba2+��Al3+��Fe2+ |
������ | SiO32-��MnO4����Cl����NO3����SO32���� |
ʵ���ȡ��������Һ��������ʵ�顣
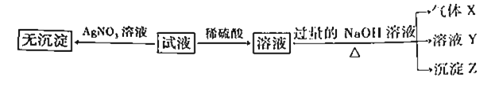
ʵ���Ϊ�˽�һ��ȷ������Һ����ɣ�ȡ100mLԭ��Һ�������Һ�еμ�1mol��L-1��NaOH��Һ����������������������������Һ����Ĺ�ϵ��ͼ��ʾ��

�ش��������⣺
��1��������ʵ��Ϳ����ƶϳ����ϱ��е�����һ�������ڵ���____________�֡�
��2��ͨ��ʵ������ȷ������Һ��һ�����ڵ���������________________��
��3��д��ʵ����ͼ����BC�ζ�Ӧ�����ӷ���ʽ��_______________________________________________________________��
��4��A���Ӧ�Ĺ�������Ϊ____________g��
��5������Һ�������ӵ�Ũ��Ϊ____________mol��L��1
����Ŀ������ع㷺Ӧ���ڻ�϶�������ϵͳ���缫������Ni(OH)2��̼�ۺ���������Ϳ���������Ƴɡ����ڵ��ʹ�ú�缫���϶Ի�����Σ����ij��ȤС��Ըõ�ص缫���Ͻ��л����о������ʵ���������£�

��֪��a.NiCl2������ˮ��Fe3����������Ni2����
b��ij�¶���һЩ�������������Ksp����ʼ��������ȫ����ʱ������pH�����ʾ��
M(OH)n | Ksp | pH | |
��ʼ���� | ������ȫ | ||
Al(OH)3 | 1.9��10��33 | 3.43 | 4.19 |
Fe(OH)3 | 3.9��10��38 | 2.53 | 2.94 |
Ni(OH)2 | 1.6��10��14 | 7.60 | 9.75 |
�ش��������⣺
��1�����ݱ��������жϲ��������������ij�����______�ͳ�����______(�ѧʽ)����pH1___pH2(������������������������)���������ֳ�������������______(�����)��
A��pH��ֽ B��ʯ��ָʾ�� C��pH��
��2����֪�ܽ�ȣ�NiC2O4��NiC2O4H2O��NiC2O42H2O���������Ļ�ѧ����ʽ��______�����������˳�������IJ���������_____________________��
��3����д�������������ӷ���ʽ____________________________________��

