题目内容
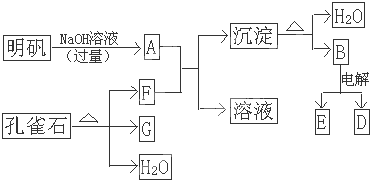
在一定条件下可实现下图所示物质之间的变化
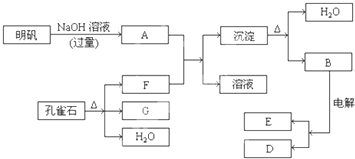
请填写以下空白:
(1)写出明矾(KAl(SO4)2?12H2O)溶液中逐步加入NaOH溶液至过量的实验现象为
(2)G物质的化学式为
(3)图中所得G和D都为固体,其混合后在高温下可发生反应,写出该反应的化学方程式
(4)电解熔融的B是工业上生产某常用金属的方法,每生成1mol D转移的电子数目为

请填写以下空白:
(1)写出明矾(KAl(SO4)2?12H2O)溶液中逐步加入NaOH溶液至过量的实验现象为
先生成白色沉淀后沉淀逐渐消失
先生成白色沉淀后沉淀逐渐消失
,反应的总离子方程式Al3++4OH-=AlO2-+2H2O
Al3++4OH-=AlO2-+2H2O
;(2)G物质的化学式为
Cu
Cu
;A和过量的F反应的离子方程式为CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-
CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-
.(3)图中所得G和D都为固体,其混合后在高温下可发生反应,写出该反应的化学方程式
2Al+3CuO
Al2O3+3Cu
| ||
2Al+3CuO
Al2O3+3Cu
;
| ||
(4)电解熔融的B是工业上生产某常用金属的方法,每生成1mol D转移的电子数目为
3NA
3NA
.分析:明矾为KAl(SO4)2?12H2O,由转化关系图可知,加入NaOH溶液至过量,先生成氢氧化铝沉淀后沉淀溶解生成偏铝酸钾,孔雀石分解生成CuO、水、CO2,F与A反应生成沉淀,则F为CO2,G为CuO,再结合图可知,B为Al2O3,D为固体,则D为Al,然后结合物质的性质及化学用语来解答.
解答:解:明矾为KAl(SO4)2?12H2O,由转化关系图可知,加入NaOH溶液至过量,先生成氢氧化铝沉淀后沉淀溶解生成偏铝酸钾,孔雀石分解生成CuO、水、CO2,F与A反应生成沉淀,则F为CO2,G为CuO,再结合图可知,B为Al2O3,D为固体,则D为Al,
(1)明矾(KAl(SO4)2?12H2O)溶液中逐步加入NaOH溶液至过量的实验现象为先生成白色沉淀后沉淀逐渐消失,反应的总离子反应为Al3++4OH-=AlO2-+2H2O,
故答案为:先生成白色沉淀后沉淀逐渐消失;Al3++4OH-=AlO2-+2H2O;
(2)由上述分析可知,G为CuO,A和过量的F反应的离子方程式为CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故答案为:CuO;CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-;
(3)G和D都在高温下可发生反应,该反应的化学方程式为2Al+3CuO
Al2O3+3Cu,故答案为:2Al+3CuO
Al2O3+3Cu;
(4)由2Al2O3
4Al+3O2↑,则电解熔融的B每生成1mol D转移的电子数目为1mol×3×NAmol-1=3NA,故答案为:3NA.
(1)明矾(KAl(SO4)2?12H2O)溶液中逐步加入NaOH溶液至过量的实验现象为先生成白色沉淀后沉淀逐渐消失,反应的总离子反应为Al3++4OH-=AlO2-+2H2O,
故答案为:先生成白色沉淀后沉淀逐渐消失;Al3++4OH-=AlO2-+2H2O;
(2)由上述分析可知,G为CuO,A和过量的F反应的离子方程式为CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故答案为:CuO;CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-;
(3)G和D都在高温下可发生反应,该反应的化学方程式为2Al+3CuO
| ||
| ||
(4)由2Al2O3
| ||
点评:本题为框图考查无机物的推断,把握明矾及孔雀石的组成及性质为解答的突破口,注意结合框图及物质的性质,直接得出物质,然后顺推或逆推或由两边向中间推得出其他物质,侧重Al及其化合物转化的考查,题目难度中等.

练习册系列答案
相关题目

 在一定条件下可实现下图所示物质之间的变化:
在一定条件下可实现下图所示物质之间的变化: