题目内容
氢氧燃料电池的基本构造如图。A、B是多孔石墨制成,通入的气体由孔隙中逸出,在电极表面得失电子。电解质溶液是KOH溶液。下列关于该电池的说法中错误的是
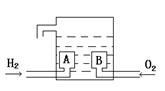
A.H2发生氧化反应 B.e-由B电极流向A电极
C.A电极为负极 D.每摩O2得到4mole-

A.H2发生氧化反应 B.e-由B电极流向A电极
C.A电极为负极 D.每摩O2得到4mole-
B
略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
题目内容


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案