题目内容
某待测液中可能含有Fe3+、Fe2+、K+、NH4+、Cl-、SO42-等离子,进行如下实验:
(1)取溶液,加入过量酸化的AgNO3溶液,有白色沉淀生成.
(2)另取溶液,加入过量的BaCl2溶液,没有白色沉淀生成.
(3)取步骤(2)中少量溶液,滴入2滴KSCN溶液,没有明显的现象出现;再滴入氯水仍无明显的现象出现.
(4)取少量步骤(3)中的溶液,加入NaOH溶液至使溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体.根据实验现象回答:待测液中一定含有______离子,一定不含有______离子,还有一种离子不能确定是否存在,要检验这种离子的实验方法是(填写实验名称和观察到的现象,不要求写实验操作过程)______.
(2)加入过量的BaCl2溶液,没有白色沉淀,据此判断溶液中没有SO42-;
(3)取步骤(2)中少量溶液,滴入2滴KSCN溶液,没有明显的现象出现,说明溶液中没有Fe3+;再滴入氯水仍无明显的现象出现,说明原溶液中没有Fe2+.
(4)铵根离子在加热条件下与氢氧化钠反应生成能使湿润的红色石蕊试纸变蓝色的氨气,这是铵根离子的特征反应,根据实验现象判断原溶液中含有NH4+;
通过以上实验不能确定原溶液中是否含有K+.要想检验是否含有钾离子,必须通过焰色反应;焰色反应的方法是:通过蓝色钴玻璃观察火焰,如果火焰呈紫色就说明有钾离子,否则没有.
故答案为:NH4+、Cl-;Fe3+、Fe2+、SO42-;焰色反应;通过蓝色钴玻璃观察火焰,火焰呈紫色.
分析:根据实验(1)判断可能存在的离子;
根据实验(2)判断不存在的离子;
根据实验(3)判断不存在的离子;
根据实验(4)判断存在的离子.
点评:本题考查了常见离子的检验,考查物质的检验有:常见阳离子的检验、常见阴离子的检验、常见气体的检验;要注意的是:焰色反应是元素的性质不是单质的性质,要观察钾元素的焰色反应时,必须透过蓝色钴玻璃,除去钠元素的干扰,才能观察到钾元素焰色反应的颜色.

(9分)用中和滴定法测定某烧碱的浓度。请回答在主要操作过程中的有关问题:
(1)将1.70g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成200mL溶液。将0.20mol/L的盐酸标准溶液装入酸式滴定管,滴定时,锥形瓶中加2—3滴 作为指示剂;滴定过程中,左手控制活塞,右手旋转摇动锥形瓶,眼睛应注视 ,
当 时即为滴定终点。有关数据如下:
| 滴定序号 | 待测溶液体积(单位:mL) | 所消耗盐酸体积(单位:mL) | ||
| 滴定前读数 | 滴定后读数 | 消耗盐酸体积 | ||
| 1 | 20.00 | 0.50 | 20.60 | V(平)= ________ |
| 2 | 20.00 | 6.00 | 26.00 | |
(3)若该学生测定值偏大了,则引起测定误差的可能原因是_______________________
A.酸式滴定管用水洗后,未用标准酸液润洗
B.酸式滴定管尖嘴部分有气泡未排除,滴定后气泡消失
C.锥形瓶用蒸馏水洗后,未用碱液洗
D.酸式滴定管起始读数俯视,滴定后读数仰视
E.在滴定过程中向锥形瓶中添加少量蒸馏水
F.取待测液时,碱式滴定管未用碱液洗
G.当指示剂局部变色时,停止滴定
某学生进行研究性学习的课题为:用中和滴定法测定某烧碱的浓度。请回答他在主要操作过程中的有关问题:
(1)配制待测溶液:将1.70g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成200mL溶液,所需的主要仪器除天平、药匙外,还有___ __、 、
、 ;
(2)滴定:①盛装0.20mol/L的盐酸标准溶液应该用________式滴定管,②滴定时,锥形瓶中加2――3滴酚酞作为指示剂,滴定过程中,一支手控制滴定管活塞,另一支手_____________,眼睛应注视__________ ______ _,当__________时即为滴定终点;③有关数据纪录如下:
滴定序号 | 待测溶液体积(单位:mL) | 所消耗盐酸体积(单位:mL) | ||
滴定前读数 | 滴定后读数 | 消耗盐酸体积 | ||
1 | 20.00 | 0.50 | 20.60 | V(平)= ________ |
2 | 20.00 | 6.00 | 26.00 | |
(3)计算:测得NaOH溶液的浓度为 ____________mol/L,烧碱样品的纯度为 _____。
(4)若该学生测定值偏大了,则该同学引起测定误差的可能原因是____________,
A.酸式滴定管用水洗后,未用标准酸液润洗
B.酸式滴定管尖嘴部分有气泡未排除,滴定后气泡消失
C.锥形瓶用蒸馏水洗后,未用碱液洗
D.酸式滴定管起始读数俯视,滴定后读数仰视
E.在滴定过程中向锥形瓶中添加少量蒸馏水
F.取待测液时,碱式滴定管未用碱液洗
G.当指示剂局部变色时,停止滴定
某学生进行研究性学习的课题为:用中和滴定法测定某烧碱的纯度。请回答他在主要操作过程中的有关问题:
(1)配制待测溶液:将1.70g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成200mL溶液,所需的主要仪器有 ;
(2)滴定:①盛装0.20mol/L盐酸标准溶液应该用 式滴定管;
②滴定时,锥形瓶中加2-3滴 作为指示剂,滴定过程中,左手 ,右手 ,两眼应注视 ,当 时即为滴定终点;
③有关数据记录如下:
| 滴定序号 | 待测验定溶液体积 (ml) | 所消耗盐酸体积(ml) | ||
| 滴定前读数 | 滴定后读数 | 消耗盐酸体积 | ||
| 1 | 20.00 | 0.50 | 20.60 | V(平)= |
| 2 | 20.00 | 6.00 | 26.00 | |
(3)计算:测得NaOH溶液的浓度为 mol/L,烧碱样品的纯度为 。
(4)若实验指导教师测得烧碱样品的准确纯度为92.5%,则该同学引起测定误差的可能原因是
A、酸式滴定管用水洗后,未用标准酸液润洗
B、酸式滴定管尖嘴部分有气泡未排除,滴定后气泡消失
C、锥形瓶用蒸馏水洗后,未用碱液洗
D、酸式滴定管,起始读数俯视,滴定后读数仰视
E、在滴定过程中,向锥形瓶中添加蒸馏水
F、取待测液时,碱式滴定管未用碱液洗
G、当指示剂局部变色时,停止滴定
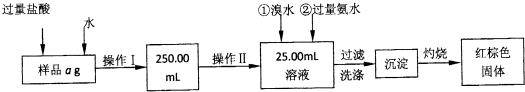
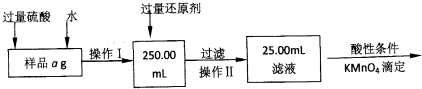
 用中和滴定法测定某烧碱的浓度.请回答主要操作过程中的有关问题:
用中和滴定法测定某烧碱的浓度.请回答主要操作过程中的有关问题: