题目内容
【题目】弱酸H2A溶液中存在H2A、HA-和A2- 三种形态的粒子,其物质的量分数 δ( X)=  随溶液pH变化的关系如图所示,下列说法正确的是( )
随溶液pH变化的关系如图所示,下列说法正确的是( )

A. 曲线①代表的粒子是HA-
B. 0.1mol·L -1的NaHA溶液中存在:c(Na+ )+c(A2- )+c(H2A)+c(HA- )>0.2 mol·L-1
C. 若图中的a值为4.2,则H2A的第二步电离平衡常数Ka1为10-4.2
D. 随着PH的升高,  的比值先增大后减小
的比值先增大后减小
【答案】C
【解析】A. 曲线①代表的粒子是H2A,②代表的粒子是HA-,③代表的粒子是A2-,故A错误;B、 根据物料守恒:0.1mol·L-1的NaHA溶液中存在:c(Na+)+c(A2-)+c(H2A)+c(HA-)=0.2mol·L-1,故B错误;C、a点有Ka1= =10-4.2,即图中的a值为4.2,则H2A的第二步电离平衡常数Ka1为10-4.2,故C正确;D、随着PH的升高,氢离子浓度减小,
=10-4.2,即图中的a值为4.2,则H2A的第二步电离平衡常数Ka1为10-4.2,故C正确;D、随着PH的升高,氢离子浓度减小,  =K/c(H+)的比值增大,故D错误;故选C。
=K/c(H+)的比值增大,故D错误;故选C。

练习册系列答案
相关题目
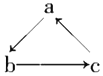
【题目】Na、Al、Fe、Cu是中学化学中重要的金属元素。它们的单质及其化合物之间有很多转化关系。下表所列物质不能按如图(“→”表示一步完成)关系相互转化的是 ( )
选项 | A | B | C | D |
|
a | Na | Al | Fe | Cu | |
b | NaOH | Al2O3 | FeCl3 | CuSO4 | |
c | NaCl | Al(OH)3 | FeCl2 | CuCl2 |
A. A B. B C. C D. D