题目内容
下列物质中σ键和π键数目比为1 :2的是
| A.O2 | B.HCN | C.CO2 | D.N2 |
D
解析试题分析:A. O2之间是非极性键,一个σ键,一个 π 键故A错。B选项HCN有四个化学键,CN三键中一个o~键两个派键,而碳氢单键是o~键故B错。C选项CO2中的C是sp杂化,两个杂化轨道分别与两个氧成σ键。C剩余两个彼此垂直的2p轨道(与C-σ键也垂直),每个轨道有一个电子,两侧的每个O原子的价轨道的三个2p轨道中,一个与C成σ键,另外两个彼此垂直,分别和C剩余p轨道平行,即O-C-O在垂直于σ键的两个方向上分别有三个p轨道平行,可形成大π键,由于每个O的两个P轨道的电子是 2,1和1,2与C的电子加起来分别是4个电子,所以形成的是π34.故C选项错误,
考点:考查化学键的相关知识点。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某学生在做元素性质与原子结构的关系的实验时,设计了一套实验方案,并记录了有关的实验现象。请帮助该学生整理并完成实验报告。
(1)实验目的。
探究同一主族元素性质的递变规律。
(2)实验用品。
仪器:试管、胶头滴管。
药品:新制氯水、新制溴水、溴化钠溶液、碘化钠溶液、四氯化碳。
(3)实验内容(在下表横线中填写相关内容)。
| 序号 | 实验方案 | 实验现象 |
| ① | 向盛有少量溴化钠溶液的试管中滴加少量新制氯水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈________色 |
| ② | 向盛有少量碘化钠溶液的试管中滴加少量新制溴水,振荡,再加入少量四氯化碳,振荡后静置 | 液体分为两层,下层呈________色 |
(4)实验结论:__________________________________________________________。
(5)问题和讨论。
①上述两个实验中发生反应的离子方程式分别为________、________。
②由于氟单质过于活泼,所以很难设计出一个简单的实验来验证其氧化性的强弱。试列举两项事实说明氟的非金属性比氯的强:________、________。
下列说法不正确的是
| A.化学反应中一定有化学键断裂,同时也有化学键形成 |
| B.含有共价键的化合物必是共价化合物 |
| C.含有阴离子的化合物一定含有阳离子 |
| D.金属元素和非金属元素形成的化合物不一定是离子化合物 |
下列表述不正确的是( )
| A.131I与127I互为同位素,化学性质几乎相同 |
| B.pm 2. 5含有铅、镉、铬、钒等对人体有害的金属元素 |
| C.除去SO2中混有的少量HCl,使气体通过盛有饱和NaHSO3溶液的洗气瓶 |
| D.为了证明氢氧化钠是离子化合物,可在瓷坩埚中将氢氧化钠固体熔化后测其导电性 |
下列对σ键的认识不正确的是
| A.ss σ键与sp σ键的对称性相同 |
| B.烯烃分子中的碳碳双键的键能是碳碳单键键能的二倍 |
| C.分子中含有共价键,则至少含有一个σ键 |
| D.含有π键的化合物与只含σ键的化合物的化学性质不同 |
下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH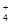 和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和C2H2 ⑥SiO
和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和C2H2 ⑥SiO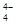 和SO
和SO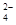
| A.全部 | B.除①④⑥以外 | C.③④⑤⑥ | D.②⑤⑥ |
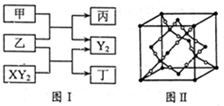
 键与π键的数目之比为_________;
键与π键的数目之比为_________;
