题目内容
【题目】下列性质比较中不正确的是( )
A.沸点:CBr4>CF4
B.水溶性:HBr>Br2
C.硬度:镁>镁铝合金
D.熔点:金刚石>NaCl
【答案】C
【解析】解:A.CBr4和CF4都是分子晶体,CBr4的相对分子质量大于CF4 , 范德华力越大,沸点越高,因此沸点CBr4>CF4 , 故A正确;B.水是极性分子,HBr是极性分子,Br2是非极性分子,根据相似相溶,水溶性HBr>Br2 , 故B正确;
C.镁铝合金的硬度比镁的硬度大,故C错误;
D.金刚石是原子晶体,NaCl是离子晶体,原子晶体的熔点大于离子晶体,因此熔点:金刚石>NaCl,故D正确;
故选C.

练习册系列答案
相关题目
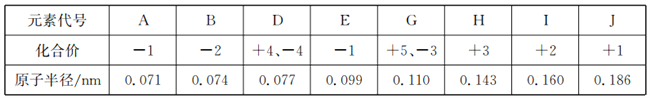
【题目】Ⅰ几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期.(请用化学用语答题)
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6﹣2 | +5﹣3 | ﹣2 | +3 |
(1)R的元素符号为; M在元素周期表中的位置为 .
(2)X与Y按原子个数比1:1构成的物质的电子式为;所含化学键类型 .
(3)X+ , Y2,M2离子半径由大到小的顺序为(用离子符号表示) .
(4)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的电极反应式 .
Ⅱ如图转化关系A ![]() B
B ![]() C,若B为白色胶状不溶物,则A与C反应的离子方程式为 .
C,若B为白色胶状不溶物,则A与C反应的离子方程式为 .