题目内容
19. 图中线段分别是A,B,C是在2L容器中的物质的量随时间的变化曲线.由图中数据分析:
图中线段分别是A,B,C是在2L容器中的物质的量随时间的变化曲线.由图中数据分析:(1)反应物是A、C,生成物是B.
(2)反应从开始到2分钟这段时间内C的平均反应速率为0.3mol/(L•min).
(3)写出该反应的化学反应方程式2A+2C?3B.
分析 (1)根据反应中反应物减小,生成物增加,结合图判断反应物和生成物;
(2)根据v=$\frac{△c}{t}$计算速率;
(3)根据反应中各物质的物质的量的变化之比等于反应中各物质计量数之比,书写化学方程式.
解答 解:(1)根据图可知,A、C随着反应的进行,物质的量减小,B随着反应的进行,物质的量增加,所以A、C是反应物,B是生成物,故答案为:A、C;B;
(2)应从开始到2分钟这段时间内△n(C)=2mol-0.8mol=1.2mol,所以C的平均反应速率v=$\frac{△c}{t}$=$\frac{\frac{1.2mol}{2L}}{2min}$=0.3mol/(L•min),故答案为:0.3mol/(L•min);
(3)根据(1)可知,A、C是反应物,B是生成物,根据图可知,应从开始到2分钟这段时间内△n(C)=2mol-0.8mol=1.2mol,△n(B)=1.8mol,△n(A)=3mol-1.8mol=1.2mol,所以△n(C):n(A):△n(B)=2:2:3,所以反应的化学方程式为2A+2C?3B,故答案为:2A+2C?3B.
点评 本题考查化学平衡图象分析题目,题目难度不大,注意分析各物质的量的变化曲线,把握化学方程式的判断方法.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
10.下列排列顺序不正确的是( )
| A. | 熔点:金刚石>金属钠>干冰 | B. | 离子半径:S2-<Cl-<K+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 热稳定性:CH4<NH3<H2O |
7.据报道:1994年11月9日德国科学家利用数亿镍原子(28Ni)对数亿个铅原子(82Pb)连续轰击数天后,制得一种新原子269X(暂用X表示),它属于一种新元素--第110号元素,这种新元素是有史以来制得的最重的元素,存在时间不到千分之一秒.则该X元素原子核内的中子数是( )
| A. | 269 | B. | 110 | C. | 159 | D. | 82 |
14.下列说法正确的是( )
| A. | 加热使氧化镁熔化不需要破坏化学键 | |
| B. | 分子间作用力比化学键强的多 | |
| C. | 加热使冰融化主要破坏分子间作用力 | |
| D. | 化学键是指物质中相邻的原子或离子间的强烈的吸引作用 |
4.从实验室用氯酸钾制取氧气后的剩余物中回收二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体)( )
| A. | 溶解、蒸发、洗涤、过滤 | B. | 溶解、过滤、蒸发、洗涤 | ||
| C. | 溶解、过滤、洗涤、干燥 | D. | 溶解、洗涤、过滤、加热 |
8.下列化学用语正确的是( )
| A. | S2-的结构示意图 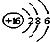 | B. | 中子数为16的硫原子:${\;}_{16}^{34}$S | ||
| C. | 羟基的电子式: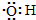 | D. | 乙烯的分子式:CH2=CH2 |
9.在一容积为5L的密闭容器中放1mol 02放电产生下列反应:3O2═2O3,一段时间后,测得有20%的O2转化为O3,若温度和体积不变,对所得气体的下列说法不正确的是( )
| A. | 平均摩尔质量为31.8g/mol | B. | 质量仍为32g | ||
| C. | 密度仍与原气体密度相同 | D. | 对氢气的相对密度大 |
 ;煤的另一种化工方法是将煤在高温条件下与水蒸气反应制造水煤气,写出该反应的化学方程式C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.
;煤的另一种化工方法是将煤在高温条件下与水蒸气反应制造水煤气,写出该反应的化学方程式C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2.