题目内容
【题目】铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(l)基态铬原子的价电子排布式为___________。
(2)CrO2C12和NaClO均可作化工生产的氧化剂或氯化剂。制备CrO2C12的反应为:
K2Cr2O7 + 3CCl4 = 2KCl+ 2 CrO2C12+ 3COCl2↑
① 上述反应式中非金属元素电负性由大到小的顺序是_______(用元素符号表示)。
② 常温下CrO2C12是一种易溶于CCl4的液体,则固态CrO2C12属于______晶体。
③ COCl2分子中所有原子均满足8电子结构,则COCl2分子中σ键和π键的个数比为_______。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的半径分别为6.9×10-2 nm 和7.8×10-2 nm,则熔点:NiO______(填“< ”、“= ”或“>” ) FeO。
④CuCl的盐酸溶液能吸收CO生成复合物氯化羰基亚铜[Cu2Cl2(CO)2·2H2O] ,其结构如图所示。下列说法不正确的是_____(填字母序号)。

A.该复合物中只含有离子键和配位键 B.该复合物中Cl原子的杂化类型为sp3
C.该复合物中只有CO和H2O作为配位体 D.CO与N2的价电子总数相同,其结构为C≡O
【答案】 3d54s1 O>Cl>C 分子 3∶1 > AC
【解析】(1)基态铬原子的电子排布式为1s22s22p63s23p63d54s1,价电子排布式为3d54s1,故答案为:3d54s1;
(2)①反应式中非金属元素有三种:O、C、Cl,它们的电负性由大到小顺序是O>Cl>C,故答案为:O>Cl>C;
②常温时CrO2Cl2为液体,说明熔点低,所以固态CrO2Cl2属于分子晶体,故答案为:分子;
③COCl2分子中有1个C=O键和2个C-Cl键,所以COCl2分子中σ键的数目为3,π键的数目为1,个数比3:1,故答案为:3:1;
(3)NiO、FeO的晶体结构类型均与氯化钠的相同,说明二者都是离子晶体,离子晶体的熔点与离子键的强弱有关,离子所带电荷数越多,离子半径越小,离子键越强,熔点越高.由于Ni2+的离子半径小于Fe2+的离子半径,属于熔点是NiO>FeO,故答案为:>;
(4)A.该复合物中存在化学键类型有离子键、配位键、极性共价键等,故A错误;B.该复合物中Cl原子的杂化类型为sp3,故B正确;C.该复合物中配位体有CO、H2O和Cl原子,故C错误;D.CO与N2属于等电子体结构相似,故结构式为C≡O,故D正确;故选AC。

 初中暑期衔接系列答案
初中暑期衔接系列答案【题目】已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行卤素的性质实验。玻璃管内分别装有滴有不同溶液的白色棉球,反应一段时间后,对图中指定部分颜色描述正确的是( )
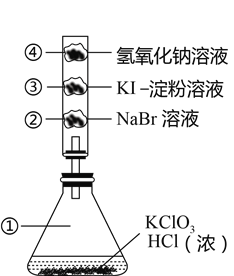
选项 | ① | ② | ③ | ④ |
A | 黄绿色 | 白色 | 紫色 | 白色 |
B | 黄绿色 | 橙色 | 紫色 | 黄绿色 |
C | 黄绿色 | 橙色 | 蓝色 | 白色 |
D | 黄绿色 | 橙色 | 蓝色 | 黄绿色 |
A. A B. B C. C D. D
【题目】有A、B、C、D、E五种元素。其相关信息如下
元素 | 相关信息 |
A | A原子的1s 轨道上只有l 个电子 |
B | B是电负性最大的元素 |
C | C的基态原子2p轨道中有三个未成对电子 |
D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答下列问题:
(1)写出E元素原子基态时的电子排布式__。
(2)C元素的第一电离能比氧元素的第一电离能_____(填“大”或“小”)。
(3)CA3分子中C原子的杂化轨道类型是__。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有_____(填序号)。
① 配位键 ② 金属键 ③ 极性共价键 ④非极性共价键 ⑤ 离子键 ⑥ 氢键
若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为_______(填字母)
a.平面正方形 b.正四面体 c.三角锥形 d. V 形
(5)B与D可形成离子化合物,其晶胞结构如下图所示。其中D离子的配位数为____, 若该晶体的密度为ag/cm3,则B与D间最短距离是______cm (写出表达式即可)。

