题目内容
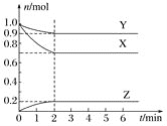
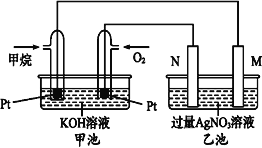
【题目】一定温度下将Cl2缓慢通入水中。当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a。已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )
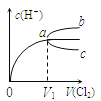
A.将饱和氯水加水稀释,溶液中c(H+)变化如曲线b
B.将饱和氯水降低温度,溶液中c(H+)变化如曲线c
C.在饱和氯水中加入NaOH使pH>7,所得溶液中存在下列关系:c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(ClO-)
D.在饱和氯水中加入NaOH使pH=7,所得溶液中存在下列关系:c(Na+)>c(ClO-)>c(Cl-)>c(HClO)
【答案】C
【解析】
A.将饱和氯水加水稀释,稀释过程中溶液中c(H+)将减小,对应曲线c,故A错误;
B.将饱和氯水降低温度,Cl2的溶解度将增大,根据![]() 可知,平衡将正向移动,溶液中c(H+)将增大,对应曲线b,故B错误;
可知,平衡将正向移动,溶液中c(H+)将增大,对应曲线b,故B错误;
C.在饱和氯水中加入NaOH,溶液中存在电荷守恒:c(Na+)+c(H+)=c(Cl-)+c(OH-)+c(ClO-),故C正确;
D.溶液pH=7时,次氯酸过量,根据氯气与水反应的特点可知溶液中存在c(Cl-)=c(HClO)+c(ClO-),因此c(Cl-)>c(ClO-),故D错误;
故答案为:C。

【题目】分别取40mL的0.50mol·L-1盐酸与40mL的0.55mol·L-1NaOH溶液进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
(1)理论上稀强酸、稀强碱反应生成1mol水时放出57.3kJ的热量,写出表示稀硫酸和稀NaOH溶液反应的中和热的热化学方程式__。
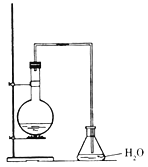
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其原因是__。
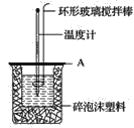
(3)假设盐酸和NaOH溶液的密度都是1g·cm-3,又知中和后生成溶液的比热容c=4.18J·g-1·℃-1。为了计算中和热,实验时还需测量的数据有(填字母)__。
A.反应前盐酸溶液的温度
B.反应前盐酸溶液的质量
C.反应前NaOH溶液的温度
D.反应前NaOH溶液的质量
E.反应后混合溶液的最高温度
F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH | ||
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=__。