题目内容
【题目】某同学用下列装置制备并检验Cl2的性质,下列说法正确的是
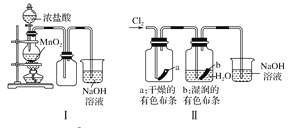
A. Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗
B. Ⅱ图中:湿润的有色布条能褪色,烧杯NaOH溶液的作用是吸收尾气
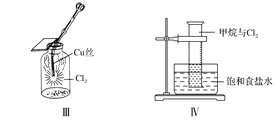
C. Ⅲ图中:生成蓝色的烟
D. Ⅳ图中:量筒中发生了加成反应,量筒内液面上升,量筒壁上有无色液滴出现
【答案】B
【解析】
A.稀盐酸与二氧化锰不反应;干燥的氯气没有漂白性,Cl2+H2O=HCl+HClO,HClO具有漂白性,氢氧化钠溶液与氯气反应生成氯化钠和次氯酸钠;氯气与铜反应生成棕黄色的烟;甲烷与氯气发生取代反应。
A.二氧化锰和浓盐酸在加热条件下发生氧化还原反应生成氯气,但稀盐酸与二氧化锰不反应,当盐酸浓度降低到一定程度时,反应停止,则盐酸不能完全消耗,故A错误;干燥的氯气没有漂白性,Cl2+H2O=HCl+HClO,HClO具有漂白性,氢氧化钠溶液与氯气反应生成氯化钠和次氯酸钠,所以Ⅱ图中:湿润的有色布条能褪色,烧杯NaOH溶液的作用是吸收尾气,故B正确;氯气与铜反应生成棕黄色的烟,故C错误;甲烷与氯气发生取代反应,故D错误。

 名校课堂系列答案
名校课堂系列答案【题目】某小组在实验室中探究金属钠与二氧化碳的反应。回答下列问题:

(1)选用如图所示装置及药品制取CO2。打开弹簧夹,制取CO2。为了得到干燥.纯净的CO2,产生的气流应依次通过盛有_________的洗气瓶(填试剂名称)。反应结束后,关闭弹簧夹,可观察到的现象是____________________________。不能用稀硫酸代替稀盐酸,其原因是______________________________。
(2)金属钠与二氧化碳反应的实验步骤及现象如下表:
步骤 | 现象 |
将一小块金属钠在燃烧匙中点燃,迅速伸入盛有CO2的集气瓶中。充分反应,放置冷却 | 产生大量白烟,集气瓶底部有黑色固体产生,瓶壁上有白色物质产生 |
在集气瓶中加入适量蒸馏水,振荡.过滤 | 滤纸上留下黑色固体,滤液为无色溶液 |
①为检验集气瓶瓶壁上白色物质的成分,取适量滤液于2支试管中,向一支试管中滴加1滴酚酞溶液,溶液变红:向第二支试管中滴加澄清石灰水,溶液变浑浊。
据此推断,白色物质的主要成分是________(填标号)。
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
②为检验黑色固体的成分,将其与浓硫酸反应,生成的气体具有刺激性气味。据此推断黑色固体是________________。
③本实验中金属钠与二氧化碳反应的化学方程式为_______________________。