题目内容
【题目】(1)苯和溴的取代反应的实验装置如图所示,其中A为具支试管改制成的反应容器,在其下端开了一小孔,塞好石棉绒,再加入少量铁屑。
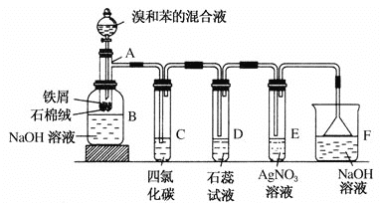
填写下列空白:
①试管A中的反应方程式为______________。
②试管C中四氯化碳的作用是:____________________________。反应开始后,观察D试管,看到的现象为:_______________。写出E中反应的离子方程式______________。
③反应2~3 min后,在B中的NaOH溶液里可观察到的现象是____________。
④在上述整套装置中,具有防倒吸功能的仪器有________(填字母)。
(2)实验室制备硝基苯的主要步骤如下:
a.配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
b.向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
c.在55~60 ℃下发生反应,直至反应结束;
d.除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤;
e.将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯。请填写下列空白:
①制备硝基苯的反应类型是________。
②配制一定比例的浓H2SO4和浓HNO3的混合酸时,操作的注意事项是:_____________。
③步骤d中洗涤、分离粗硝基苯应使用的仪器是_________________。
④步骤d中粗产品用5%NaOH溶液洗涤的目的是___________________。
【答案】![]() +Br2
+Br2![]() +HBr 除去HBr中的溴蒸气 D试管中石蕊试液慢慢变红,导管口有白雾产生 Ag++Br-=AgBr↓ 试管底部有无色油状液体 D、E、F 取代反应 先将浓硝酸注入容器中再慢慢加入浓硫酸,并及时搅拌 分液漏斗 除去粗产品中残留的酸
+HBr 除去HBr中的溴蒸气 D试管中石蕊试液慢慢变红,导管口有白雾产生 Ag++Br-=AgBr↓ 试管底部有无色油状液体 D、E、F 取代反应 先将浓硝酸注入容器中再慢慢加入浓硫酸,并及时搅拌 分液漏斗 除去粗产品中残留的酸
【解析】
(1)苯与液溴在催化剂作用下发生取代反应产生溴苯和溴化氢,B中用NaOH溶液除去溴苯中未反应的Br2单质;用有机溶剂四氯化碳除去气体中挥发的溴蒸气、苯,其中的溴化氢溶于石蕊试液,使石蕊试液变为红色;HBr还会与AgNO3溶液发生反应产生AgBr浅黄色沉淀,最后用NaOH溶液进行尾气处理,用倒扣的漏斗可以防止倒吸现象的发生。
(2)①浓硫酸与浓硝酸混合放出大量的热,配制混酸应将浓硫酸中注入浓硝酸中,及时搅拌、冷却,防止溅出伤人;
②分离互不相溶的液体,采取分液操作,需要用分液漏斗;
③制备的硝基苯中混有硫酸、硝酸,可以用5% NaOH溶液洗涤.
(1)①试管A中苯与液溴在Fe存在下发生取代反应,产生溴苯和HBr,反应的化学方程式为![]() ;
;
②试管C中四氯化碳的作用是除去HBr中的溴蒸气及苯;反应开始后,反应产生的HBr溶解在石蕊试液中,HBr溶解电离产生H+、Br-,溶液显酸性,观察D试管中溶液由紫色变为红色;逸出的HBr遇空气中的水蒸气形成HBr的小液滴,因此会看到导管口有白雾产生;在E中HBr与AgNO3溶液发生复分解反应,产生淡黄色AgBr和HNO3,反应的离子方程式为Ag++Br-=AgBr↓;
③反应2~3 min后,反应产生溴苯,未反应的单质Br2与B中的NaOH溶液发生反应产生NaBr、NaBrO和H2O,而溴苯是不能溶解于水的液体,密度比水大,故可观察到的现象是液体分层,在试管底部有无色油状液体;
④装置D和E导管口在液面上方,能防止倒吸,装置F中倒置漏斗增大了气体与氢氧化钠溶液的接触面积,有缓冲作用,能够防止倒吸,故在上述整套装置中,具有防倒吸功能的仪器有D、E、F;
(2)①苯与浓硝酸在浓硫酸存在时,在加热条件下发生取代反应产生硝基苯和水,因此制备硝基苯的反应类型是取代反应;
②浓硫酸与浓硝酸混合放出大量的热,配制混酸操作注意事项是:先将浓硝酸注入容器中,再慢慢注入浓硫酸,并及时搅拌和冷却;
③硝基苯是油状液体,与水不互溶,分离互不相溶的液态混合物,采取分液方法,需要用的玻璃仪器是分液漏斗;
④反应得到硝基苯粗产品中有残留的硝酸及硫酸,可以根据硝酸、硫酸具有酸性,能够与碱反应产生盐和水,而硝基苯不能溶于水,用氢氧化钠溶液洗涤除去粗产品中残留的酸。

 云南师大附小一线名师提优作业系列答案
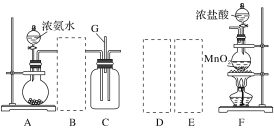
云南师大附小一线名师提优作业系列答案【题目】某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。
备选装置 | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
请回答下列问题:
(1)装置F中发生反应的离子方程式是___________________________________。
(2)装置A中的烧瓶内固体可选用________(填字母)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从如图的备选装置中选择,并将编号填入下列空格:
B:________、D:________、E:________。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:____________________________________;
(5)装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案确定该白色固体中的阳离子:_______________________________________