题目内容
11.在密闭容器中,对于反应:2SO2(g)+O2(g)?2SO3(g),下列操作能增大反应速率并使平衡右移的是( )| A. | 降低体系温度 | B. | 增大体系容积 | C. | 移去SO3 | D. | 通入O2 |
分析 根据外界条件对化学反应速率的影响分析,增大浓度、升高温度、增大压强、使用催化剂等可以加快反应速率,结合平衡移动原理分析解答.
解答 解:A.降低温度平衡向正反应方向移动,但反应速率减慢,故A不符合;
B.增大体系容积即减小压强平衡向逆反应方向移动,反应速率减慢,故B不符合;
C.移去SO3,平衡右移,但生成物浓度减小,反应速率减小,故C不符合;
D.通入氧气,氧气浓度增大,反应速率加快,平衡向正反应方向移动,故D符合;
故选D.
点评 本题考查外界条件对化学反应速率与化学平衡的影响,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
2.为了除去括号内的杂质,其试剂选择和分离方法都正确的是( )
| 序号 | 物质(杂质) | 所用试剂 | 分离方法 |
| A | 溴苯(Br2) | 苯 | 萃取、分液 |
| B | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| C | CH4(C2H4) | 酸性高锰酸钾 | 洗气 |
| D | 硝基苯(硝酸) | 氢氧化钠溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
6.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2 L二氯甲烷( CH2Cl2)所含的分子数为0.5NA | |
| B. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| C. | 1mol羟基(-OH)所含的电子总数为10NA | |
| D. | 10g质量分数为46%的乙醇溶液中,氢原子的总数为1.2NA |
16.分子式为C3H6O3的有机物,在一定条件下具有下列性质:①在浓硫酸作用下,能分别与C2H5OH和CH3COOH反应;②在浓硫酸作用下,能生成一种分子式为C6H8O4的六元环状化合物.据此,可确定C3H6O3有机物的结构简式为( )
| A. | HOCH2CH2COOH | B. | CH3CH(OH)COOH | C. | CH3OCH2COOH | D. | CH3CH(OH)CH2COOH |
3.下列化学用语表示正确的是( )
| A. | ${\;}_{12}^{24}$Mg和${\;}_{12}^{26}$Mg互为同位素 | B. | 氯原子的结构示意图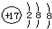 | ||
| C. | 氯化钠的电子式是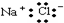 | D. | 乙酸与乙醇互为同分异构体 |


 ,
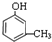
,
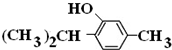 +3H2$→_{△}^{Ni}$
+3H2$→_{△}^{Ni}$
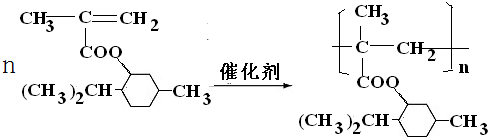 ;.
;.