题目内容
(15分)微粒A、B、C为分子,D和F为阳离子,E为阴离子,它们都含有l0个电子;B溶于A后所得的物质可电离出D和E;C是重要的化石能源。将A、B和含F离子的物质混合后可得D和一种白色沉淀。G3+离子与Ar原子的电子层结构相同。请回答:
⑴基态G原子的外围电子排布式是 。在A、B、C这三种分子中,属于非极性分子的有 (写化学式)。
⑵下列有关B的说法中正确的是 。(填字母)
a.在配合物中可作为配体
b.该分子的稳定性与氢键有关
c.分子中各原子最外层均为8e-的稳定结构
d.含1 molB的液体中有3mol氢键
⑶根据等电子体原理,D离子的空间构型是 ,其中心原子轨道的杂化类型是 。
⑷构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,上图立方体中心的“●”表示该晶体中的一个原子,请在该立方体的顶点上用“●”表示出与之紧邻的原子。
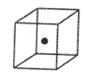
⑸光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在 。(填字母)
a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.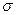 键 h.
键 h.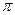 键
键
⑴基态G原子的外围电子排布式是 。在A、B、C这三种分子中,属于非极性分子的有 (写化学式)。
⑵下列有关B的说法中正确的是 。(填字母)
a.在配合物中可作为配体
b.该分子的稳定性与氢键有关
c.分子中各原子最外层均为8e-的稳定结构
d.含1 molB的液体中有3mol氢键
⑶根据等电子体原理,D离子的空间构型是 ,其中心原子轨道的杂化类型是 。
⑷构成C的中心原子可以形成多种单质,其中有一种为空间网状结构,上图立方体中心的“●”表示该晶体中的一个原子,请在该立方体的顶点上用“●”表示出与之紧邻的原子。

⑸光谱证实F与烧碱溶液反应有Na[F(OH)4]生成,则Na[F(OH)4]中不存在 。(填字母)
a.金属键 b.离子键 c.非极性键 d.极性键 f.配位键 g.
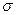 键 h.
键 h.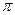 键
键 1)3d14s2 (2分)CH4(2分)(2)a (2分)(3)正四面体(2分) sp3(2分)
(4)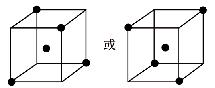 (3分) (5)ach(2分)
(3分) (5)ach(2分)
(4)
 (3分) (5)ach(2分)
(3分) (5)ach(2分)略

练习册系列答案
相关题目

 (1)写出三种元素的符号:A B______ C______
(1)写出三种元素的符号:A B______ C______ 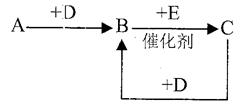
 一定能大量共存的离子组是 (填序号)。
一定能大量共存的离子组是 (填序号)。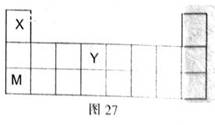
 含放射性物质超标的水和食物,不会对人体产生危害
含放射性物质超标的水和食物,不会对人体产生危害 化
化