题目内容
10.电负性的大小也可以作为判断金属性和非金属性强弱的尺度,下列关于电负性的变化规律正确的是( )| A. | 周期表中同周期元素从左到右,元素的电负性逐渐增大 | |
| B. | 周期表中同主族元素从上到下,元素的电负性逐渐增大 | |
| C. | 电负性越大,金属性越强 | |
| D. | 电负性越小,非金属性越强 |
分析 元素的非金属性越强,电负性越大,元素的金属性越强,电负性越小,结合同周期、同主族元素性质的递变规律分析.
A.周期表中从左到右非金属性逐渐增强,主族元素的电负性逐渐变大;
B.周期表中从上到下,金属性增强,所以同一主族元素的电负性逐渐减小;
C.元素的电负性越小,则元素的非金属性越弱;
D.根据电负性与元素性质的关系分析.
解答 解:A.元素的非金属性越强,电负性越大,周期表中从左到右非金属性逐渐增强,所以主族元素的电负性逐渐变大,故A正确;
B.元素的非金属性越强,电负性越大,周期表中从上到下,金属性增强,所以同一主族元素的电负性逐渐减小,故B错误;
C.元素电负性越大,原子对键合电子吸引力越大,则元素非金属性越强,故C错误;
D.元素的电负性越大,越易得电子,元素的非金属性越强,元素的电负性越小,则元素的非金属性越弱,故D错误;
故选A.
点评 本题考查了电负性的含义,题目难度不大,注意根据电负性的含义进行剖析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.有机物Q的分子式为C10H12O3,属于芳香族化合物,且有两个取代基,一定条件下Q遇足量NaHCO3、Na均能产生气体,且生成气体体积比(同温同压)为1:1,分子结构中环上的一氯代物只有两种,则Q的结构最多有( )
| A. | 19种 | B. | 10种 | C. | 16种 | D. | 12种 |
18.下列说法正确的是( )
| A. | 碳水化合物都符合通式Cn(H2O)m | |
| B. | 符合通式Cn(H2O)m的物质都是糖类 | |
| C. | 糖类物质都有甜味 | |
| D. | 糖类是人类维持生命的六大营养素之一 |
2.如图表示的是向MgCl2、AlCl3的混合溶液中开始时滴加试剂A,之后改滴试剂B,所得沉淀y(mol)与加入试剂体积V(mL)之间的关系.以下结论不正确的是( )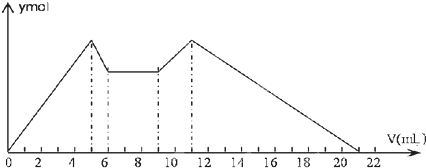

| A. | A是盐酸,B是NaOH溶液,且c(B)=2c(A) | |
| B. | 原混合液中c(Al3+):c(Mg2+):c(Cl-)=1:1:5 | |
| C. | A是NaOH溶液,B是盐酸,且c(NaOH):c(HCl)=2:1 | |
| D. | 从7到9,反应的离子方程式:H++OH-═H2O |
19.不能说明氯元素的非金属性比硫元素强的事实是( )
| A. | Cl2与H2S溶液发生置换反应 | B. | 受热时H2S能分解,HCl则不能 | ||
| C. | 单质硫可在空气中燃烧,Cl2不能 | D. | 溶于水时HCl是强酸,H2S是弱酸 |
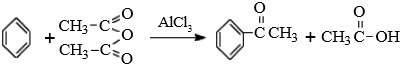
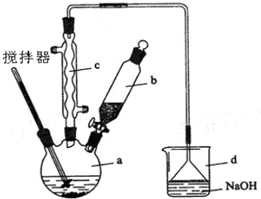
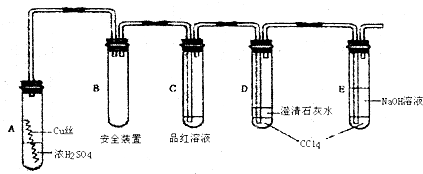
 (一)石油分馏可以得到汽油.汽油是低沸点的烷烃的混合物,其分子中的碳原子数一般在C5~C12范围内,如戊烷,其分子式为C5H12,石油分馏属于物理变化(填“化学”或“物理”).
(一)石油分馏可以得到汽油.汽油是低沸点的烷烃的混合物,其分子中的碳原子数一般在C5~C12范围内,如戊烷,其分子式为C5H12,石油分馏属于物理变化(填“化学”或“物理”).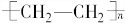 .
.