题目内容
【题目】含Ti化合物在工业生产中有着重要用途。TiCl3是烯烃定向聚合的催化剂、TiCl4可用于制备金属Ti。
nCH3CH=CH2 ![]()
![]()
TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
TiO2+2C+2Cl2![]() TiCl4+2CO
TiCl4+2CO
(1)Ti3+的基态核外电子排布式为__________;
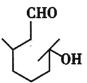
(2)丙烯分子中,碳原子轨道杂化类型为__________;
(3)Mg、Al、Cl第一电离能由大到小的顺序是___________;
(4)写出一种由第2周期元素组成且与CO互为等电子体的阴离子的电子式____;
(5)TiCl3浓溶液中加入无水乙醚,并通入HCl至饱和,在乙醚层得到绿色的异构体,分别是[Ti(H2O)6]Cl3、[Ti(H2O)5Cl]Cl2·H2O。1mol[Ti(H2O)6]Cl3中含有σ键的数目为______;
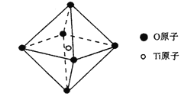
(6)钛酸锶具有超导性、热敏性等优点,该晶体的晶胞中Sr位于晶胞的顶点,O位于晶胞的面心,Ti原子填充在O原子构成的正八面体空隙的中心位置(如图),据此推测,钛酸锶的化学式为_________。
【答案】[Ar]3d1 sp2、sp3 Cl>Mg>Al ![]() 或
或![]() 18 mol SrTiO3
18 mol SrTiO3
【解析】
本题主要考查物质的结构与晶胞计算。
(1)Ti是22号元素,其原子核外有22个电子,Ti元素失去4s能级上2个电子、3d能级上电子生成![]() ,根据构造原理书写
,根据构造原理书写![]() 的基态核外电子排布式。
的基态核外电子排布式。
(2)丙烯中存在C=C-C,双键C中σ键为3,单键C的σ键为4,均不含孤对电子。
(3)同周期随原子序数增大,第一电离能呈增大趋势,元素原子各轨道为半满、全满、全空时,能量较低,第一电离能高于同周期相邻元素的。
(4)价电子数相等、原子个数相等的微粒为等电子体。
(5)在配合物[Ti(H2O)6]Cl3中,6个水分子与钛离子之间有6个配位键,为σ键,每个水分子内有2个单键,也是σ键,所以每个配合物中的配位键数为![]() 。
。
(6)该晶体的晶胞中Sr位于晶胞的顶点,则该晶胞中Sr原子个数=![]() ,O位于晶胞的面心,则O原子个数=
,O位于晶胞的面心,则O原子个数=![]() ,Ti原子填充在O原子构成的正八面体空隙的中心位置,个数为1,据此推测钛酸锶的化学式。
,Ti原子填充在O原子构成的正八面体空隙的中心位置,个数为1,据此推测钛酸锶的化学式。
(1)Ti是22号元素,其原子核外有22个电子,Ti元素失去4s能级上2个电子、3d能级上电子生成Ti3+,根据构造原理书写Ti3+的基态核外电子排布式为![]() 。
。
故答案为:![]() ;
;
(2)丙烯中存在C=CC,双键C中σ键为3,单键C的σ键为4,均不含孤对电子,杂化类型分别为![]() 、
、![]() 。
。
故答案为:![]() 、
、![]() ;
;
(3)同周期随原子序数增大,第一电离能呈增大趋势,元素原子各轨道为半满、全满、全空时,能量较低,第一电离能高于同周期相邻元素的,所以第一电离能Cl>Mg>Al。
故答案为:Cl>Mg>Al。
(4)由第二周期主族元素组成的且与CO互为等电子体的阴离子的电子式为,![]() 。
。
故答案为:![]() ;
;
(5)在配合物[Ti(H2O)6]Cl3中,6个水分子与钛离子之间有6个配位键,为σ键,每个水分子内有2个单键,也是σ键,所以每个配合物中的配位键数为![]() ,所以1mol配合物中含σ键的数目为18mol。
,所以1mol配合物中含σ键的数目为18mol。
故答案为:18mol;
(6)该晶体的晶胞中Sr位于晶胞的顶点,则该晶胞中Sr原子个数=![]() ,O位于晶胞的面心,则O原子个数=
,O位于晶胞的面心,则O原子个数=![]() ,Ti原子填充在O原子构成的正八面体空隙的中心位置,个数为1,则Sr、O、Ti原子个数为1:3:1,据此推测钛酸锶的化学式SrTiO3。
,Ti原子填充在O原子构成的正八面体空隙的中心位置,个数为1,则Sr、O、Ti原子个数为1:3:1,据此推测钛酸锶的化学式SrTiO3。
故答案为:SrTiO3。

【题目】(1)25 ℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
热化学方程式 | 平衡常数 | |
① | 2NO2(g)+NaCl(s) | K1 |
② | 4NO2(g)+2NaCl(s) | K2 |
③ | 2NO(g)+Cl2(g) | K3 |
则该温度下,ΔH3=_______________kJmol-1;K3=_____________(用K1和K2表示)。
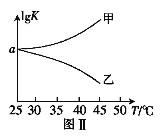
(2)25℃时,在体积为2L的恒容密闭容器中通入0.08 mol NO和0.04 molCl2发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图Ⅰ实线所示,则ΔH3 ___(填“>”“<”或“=”)0;若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是_____________;在5 min时,再充入0.08 mol NO和0.04 molCl2,则混合气体的平均相对分子质量将_____________(填“增大”、“减小”或“不变”)。图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(lgK)与温度的变化关系图,其中正确的曲线是______(填“甲”或“乙”),a值为__________。25 ℃时测得反应③在某时刻,NO(g)、Cl2(g)、NOCl(g)的浓度分别为0.8、0.1、0.3,则此时v正_________v逆(填“>”“<”或“=”)

(3)在300 ℃、8 MPa下,将CO2和H2按物质的量之比1∶3 通入一密闭容器中发生CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=_____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
CH3OH(g)+H2O(g)中反应,达到平衡时,测得CO2的平衡转化率为50%,则该反应条件下的平衡常数为Kp=_____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。