题目内容
1g碳与适量水蒸气反应生成CO和H2,需吸收10.94kJ热量,此反应的热化学方程式为( )
| A.C + H2O ="=" CO + H2ΔH= +131.28kJ·mol-1 |
| B.C(s)+ H2O(g) ="=" CO(g) + H2(g)ΔH= +10.94 kJ·mol-1 |
| C.C(s)+ H2O(l) ="=" CO(g) + H2(g)ΔH= +131.28kJ·mol-1 |
| D.C(s)+ H2O(g) ="=" CO(g) + H2(g)ΔH= +131.28kJ·mol-1 |
D
碳和水蒸气反应是吸热反应,所以△H大于0。根据题意可知1mol碳即12g碳吸热是10.94kJ×12=131.28kJ,因此选项D正确,A没有注明物质的状态,B中反应热不正确,C中水的状态不是气态,答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
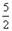 O2=2CO2(g)+H2O(l) △H=-1300kJ/mol的说法中,正确的是( )
O2=2CO2(g)+H2O(l) △H=-1300kJ/mol的说法中,正确的是( )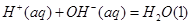

 的氢氟酸与0.1mol/L
的氢氟酸与0.1mol/L O2(g) =CO2(g),△H=-283.0 kJ·mol-1
O2(g) =CO2(g),△H=-283.0 kJ·mol-1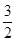 N2(g) +2H2O(g )△H=" -1135.7" kJ? mol-1
N2(g) +2H2O(g )△H=" -1135.7" kJ? mol-1