题目内容
【题目】已知难溶电解质在水溶液中存在溶解平衡MmAn(s)![]() mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。
mMn+(aq)+nAm-(aq),Ksp=cm(Mn+)·cn(Am-)称为溶度积。
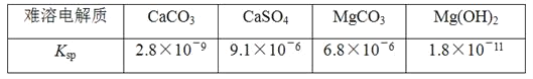
某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料(25℃):
他们的实验步骤如下:
①往100mL0.1mol·L-1的CaCl2溶液中加入0.1mol·L-1的Na2SO4溶液100mL立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO33g,搅拌,静置后弃去上层清液。
③再加入蒸馏水搅拌,静置后再弃去上层清液。
④___________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越__(填“大”或“小”)。
(2)写出第②步发生反应的化学方程式__。
(3)设计第③步的目的是什么__。
(4)请补充第④步操作及发生的现象__。
(5)请写出该转化在实际生活、生产中的一个应用__。
【答案】大 Na2CO3(aq)+CaSO4(s)![]() CaCO3(s)+Na2SO4(aq) 洗去沉淀上附着的SO42- 向沉淀中加入足量的盐酸,沉淀完全溶解,有气泡产生 将锅炉水垢中的CaSO4转化为CaCO3,易于除去
CaCO3(s)+Na2SO4(aq) 洗去沉淀上附着的SO42- 向沉淀中加入足量的盐酸,沉淀完全溶解,有气泡产生 将锅炉水垢中的CaSO4转化为CaCO3,易于除去
【解析】
(1)根据Ksp的含义分析;
(2)硫酸钙与碳酸钠反应生成碳酸钙沉淀;
(3)上层清液里有Na2SO4,所以沉淀上有附着的硫酸根离子,要洗去;
(4)检验生成的沉淀是不是碳酸钙;
(5)工厂大型锅炉除水垢的方法;
(1)Ksp越大,饱和溶液中离子的浓度越大,电解质的溶解度越大;
(2)根据表格数据,硫酸钙的Ksp比碳酸钙大,当加入碳酸钠时会反应生成碳酸钙沉淀,其反应方程式为:Na2CO3(aq)+CaSO4(s)=Na2SO4(aq)+CaCO3(s);
(3)上层清液里有Na2SO4,故应洗去沉淀上附着的SO42;
(4)因为前面加入了固体Na2CO3,生成CaCO3,向沉淀中加入足量的盐酸,如果沉淀完全溶解并放出无色无味气体,说明该沉淀是碳酸钙,说明CaSO4加入碳酸钠后生成了碳酸钙;
(5)在实际生活生产中,利用沉淀的转化可将锅炉水垢中的CaSO4转化为CaCO3,再用盐酸溶解除去。

 金钥匙试卷系列答案
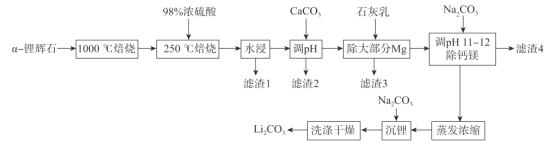
金钥匙试卷系列答案【题目】锂辉石(主要成分为LiAl(SiO3)2,还含有Fe2O3、MgO、Al2O3等杂质)是最重要的提锂矿石原料,工业上以![]() -锂辉石为原料制备碳酸锂,其工艺流程如下:
-锂辉石为原料制备碳酸锂,其工艺流程如下:
已知:①![]() -锂辉石化学惰性大,除HF外,几乎不与任何酸碱反应,
-锂辉石化学惰性大,除HF外,几乎不与任何酸碱反应, ![]() -锂辉石在高温下可转化为β一锂辉石,β一锂辉石具有更高的化学活性。
-锂辉石在高温下可转化为β一锂辉石,β一锂辉石具有更高的化学活性。
②β一锂辉石可与浓硫酸发生反应:2β一LiAl(SiO3)2+ H2SO4(浓)![]() Li2SO4 +Al2O3·4SiO2·H2O。
Li2SO4 +Al2O3·4SiO2·H2O。
③部分金属氢氧化物开始沉淀和完全沉淀的pH如表:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
请回答下列问题:
(1)将LiAl(SiO3)2改写成氧化物的形式为_______,1000 °C焙烧![]() -锂辉石的目的为_____.
-锂辉石的目的为_____.
(2)滤渣2的主要成分为________调节pH值的范围为________。
(3)“除大部分Mg”步骤的离子方程式为______________。
(4)实验室蒸发浓缩操作中所需的仪器为酒精灯、铁架台(带铁圈)、______________。
(5)洗涤过程中检验沉淀是否洗涤干净的操作为________________________________。
(6)碳酸锂是制备锂离子电池的原料之一,某锂离子电池以CoP3作为负极材料,以LiM1.5Ni0.5O4作为正极材料,以可传导Li+的无机固体电解质c-LATP作为电解液,其工作时电池反应为Li1-x Mn0.5Ni0.5O4 + Lix(CoP3 )![]() LiMn1.5Ni0.5O4+(CoP3),则该电池放电时负极的电极反应式为_________________,充电时阳极的电极反应式为_____________。
LiMn1.5Ni0.5O4+(CoP3),则该电池放电时负极的电极反应式为_________________,充电时阳极的电极反应式为_____________。