题目内容
【题目】在一定条件下,在容积为2L的恒容密闭容器中,将2molN气体和3molM气体相混合,发生如下反应:2N(g)+3M(g)![]() xQ(g)+3R(g),4s后该反应达平衡时,生成2.4molR,并测得Q的反应速率为0.1mol/(L·s),下列有关叙述正确的是
xQ(g)+3R(g),4s后该反应达平衡时,生成2.4molR,并测得Q的反应速率为0.1mol/(L·s),下列有关叙述正确的是
A. N的转化率为80% B. 0~4s内,混合气体的平均相对分子质量不变
C. x值为2 D. 平衡时M的浓度为0.6mol/L
【答案】A
【解析】
A.根据化学方程式中计量数之比,结合R的物质的量,计算参加反应N的物质的量,N的转化率=![]() ×100%;
×100%;
B.根据生成的R的物质的量,利用物质的量之比等于化学计量数之比计算生成的Q的物质的量,确定反应为气体体积缩小的反应,随着反应的进行混合气体的平均分子质量减小;
C.根据v=cVt计算生成Q的物质的量,结合R的物质的量,利用物质的量之比等于化学计量数之比计算x的值;
D.根据生成的R的物质的量,利用物质的量之比等于化学计量数之比计算参加反应的M的物质的量,M的平衡浓度=![]() 。
。
A.平衡时生成R为2.4mol,参加反应的N的物质的量为![]() 1.6mol,则N的转化率为
1.6mol,则N的转化率为![]() ×100%=80%,选项A正确;
×100%=80%,选项A正确;
B、平衡时生成的Q的物质的量为0.1mol/(L·s)×2L×4s =0.8mol,生成R为2.4mol,物质的量之比等于化学计量数之比,故0.8mol:2.4mol=x:3,解得x=1,反应为气体体积的缩小的反应,0~4s内,随着反应的进行,气体的总物质的量减小,混合气体的平均相对分子质量减小,选项B错误;
C.平衡时生成的Q的物质的量为0.1mol/Ls×2L×4s=0.8mol,生成R为2.4mol,物质的量之比等于化学计量数之比,故0.8mol:2.4mol=x:3,解得x=1,选项C错误;
D.反应达到平衡时,生成2.4molR,由方程式可知,参加反应的M的物质的量为2.4mol,故平衡时M的物质的量为3mol-2.4mol=0.6mol,M的平衡浓度为=![]() 0.3mol/L,选项D错误;
0.3mol/L,选项D错误;
答案选A。

【题目】保护环境,提倡“低碳生活”,是我们都应关注的社会问题。
(1)目前,一些汽车已改用天然气(CNG)做燃料,以减少对空气污染。
①16g甲烷完全燃烧生成液态水放出890kJ热量,则甲烷燃烧的热化学方程式是__________。
②1mol碳完全燃烧生成二氧化碳气体放出393.5kJ热量,通过计算比较,填写下列表格(精确到0.01):
物质质量1g | 燃烧放出的热量/kJ | 生成CO2的质量/g |
碳 | 32.80 | ____________ |
甲烷 | ____________ | 2.75 |
根据表格中的数据,天然气与煤相比,用天然气做燃料的优点是__________。
(2)为了减少二氧化碳的排放,利用海藻可将二氧化碳、氢气转化成水及一种可以再生的绿色能源乙醇,该反应的化学方程式是______________________________。
【题目】I.常温下0.1mol·L-1的盐酸和pH=1的醋酸各100mL分别与足量的锌粒反应,产生的气体前者比后者_____(填“>”“<”或“=”)。
II.现有常温下pH=2的HCl溶液甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)常温下0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是_____。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)c(OH-) D.c(OH-)/c(H+)
(2)取10mL的乙溶液,加入等体积的水,CH3COOH的电离平衡________(填“向左”“向右”或“不”)移动;另取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后溶液体积保持不变),待固体溶解后,溶液中c(H+)/c(CH3COOH)的比值将________(填“增大”“减小”或“无法确定”)。
(3)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗NaOH溶液体积的大小关系为V(甲)__ V(乙) (填“>”“<”或“=”)。
(4)已知25℃时,下列酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.8×10-5 | K1=4.3×10-7 K2=4.7×10-11 | 3.0×10-8 |
下列四种离子结合H+能力最强的是________。
A.HCO3— B.CO32— C.ClO- D.CH3COO-
写出下列反应的离子方程式:HClO+Na2CO3(少量):______________________。
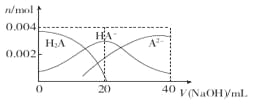
Ⅲ.室温下,0.1 mol·L-l的KOH溶液滴10.00mL 0.10 mol·L-l H2C2O4 (二元弱酸)溶液,所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和)。请回答下列问题:

(1)点③所示溶液中所有离子的浓度由大到小的顺序为:_____________________。
(2)点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4)+c(C2O42)=________mol/L。