题目内容
Ⅰ、(1)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵,则①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号) 。
(2)已知某温度下,纯水中的C(H+)=5×10-7mol/L,则此时溶液的C(OH-)为 mol/L;若温度不变,将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= 。
Ⅱ、在一个容积固定的密闭容器中,要求通过调节体系的温度使反应A(g)+2B(g)![]() 2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
⑴若x=5.5时,需要降低体系温度使反应在平衡时达到题设条件,则正反应是 热反应。
⑵欲使反应维持向逆反应方向移动,则x的取值范围为 。
⑶在一定温度下的上述平衡体系中,另按1∶2的物质的量之比充入D、E两种气体(此时容器中的气体的总物质的量不要求保持12mol),按D(g)+E(g)![]() 2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
Ⅰ、(1)④②③① (2)5×10-7 18:7
Ⅱ、(1)放热 (2)2.5<x<3.5 (3)2m+n/2
解析:
Ⅰ、(1)这四种溶液中,其中①、②、③对水的电离起到抑制作用,只有④对水的电离起到促进作用,所以④中H+浓度大,由水的离子积可计算①中C(H+)=5×10-14mol/L、②C(H+)>10-13mol/L、③C(H+)=10-13mol/L,所以四种溶液中由水电离出的H+浓度由大到小的顺序是④②③①。
(2)纯水显中性,所以C(H+)= C(OH-)或者由水的电离方程式知,水电离的C(H+)= C(OH-),所以纯水中的C(OH-)= C(H+)=5×10-7mol/L。若温度保持不变,则KW=25×10-14,依题可列等式: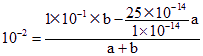 ,解得
,解得![]() 。
。
Ⅱ、(1)若x=5.5,则加入物质总的物质的量为6.5﹢5.5+2=14mol>12mol,则降温平衡右移,正反应为放热反应。
(2)依题意,平衡逆向移动,且保持容器内气体的总物质的量为12mol,则有6.5﹢x+2<12mol, x的取值为x<3.5mol;又因为该反应是可逆反应,不可能进行到底,即反应物不可能完全转化,当反应逆向进行时,假使2.0molC完全转化,将得到1molA和2molB,则有(6.5+1)+(x+2)=12mol,解x=2.5mol。综上所述,得x的取值范围为2.5<x<3.5。
(3)经分析在恒温恒容条件下,D、E两种气体按1∶2的物质的量之比充入,和向容器中投入m molD,n molF和一定物质的量的E,达到平衡状态时,D的体积分数相等,这两个平衡状态是等效平衡。依题可得以下①②③为等效平衡:
D(g) + E(g) ![]() 2F(g)
2F(g)
① x 2x 0
② m y n
③ m+0.5n y+0.5n 0
则有关系式: (m+0.5n):(y+0.5n )=x:2x=1 :2
解得 y=2m+0.5n

 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。
2F(g)发生反应。当反应达到平衡时,D在这三种物质的混合体系中的体积分数为p%。若向容器中投入m molD,n molF和一定物质的量的E,在这三种物质的新的平衡体系中,D的体积分数仍为p%,则所投入E的物质的量为 (用m、n表示;设A、B、C和D、E、F之间均不发生反应)。 2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。
2C( g)达到平衡时,保持容器内气体的总物质的量为12mol。现向反应容器中加入6.5molA,xmolB,2.0molC。