题目内容
(10分)直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示S形成硫酸酸雨的反应方程式 , 。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 。
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣),n(HSO3﹣)变化关系如下表:
①上表判断NaHSO3溶液显 性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
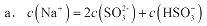
(4)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如下:
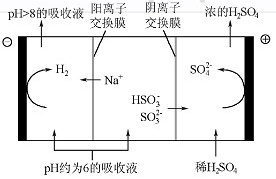
①HSO3-在阳极放电的电极反应式是 。
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用。简述再生原理:
。
(1)用化学方程式表示S形成硫酸酸雨的反应方程式 , 。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式是 。
(3)吸收液吸收SO2的过程中,pH随n(SO3²﹣),n(HSO3﹣)变化关系如下表:
| n(SO3²﹣):,n(HSO3﹣) | 91:9 | 1:1 | 1:91 |
| PH | 8.2 | 7.2 | 6.2 |
②当吸收液呈中性时,溶液中离子浓度关系正确的是(选填字母):
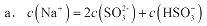
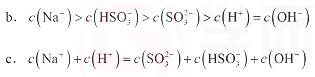
(4)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如下:

①HSO3-在阳极放电的电极反应式是 。
②当阴极室中溶液PH升至8以上时,吸收液再生并循环利用。简述再生原理:
。
(1)SO2+H2O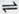 H2SO3 2H2SO3+O2
H2SO3 2H2SO3+O2 2H2SO4
2H2SO4
(2)2OH-+ SO2=H2O+SO32-
(3)①酸性 HSO3-存在:HSO3-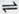 H++SO32-和HSO3-+H2O
H++SO32-和HSO3-+H2O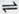 H2SO3+OH-,HSO3-的电离程度强于水解程度。 ②a b
H2SO3+OH-,HSO3-的电离程度强于水解程度。 ②a b
(4)①HSO3-+H2O-2e-= SO42-+3H+
②H+在阴极得电子生成H2,溶液中c(H+)降低,促使HSO3-电离生成SO32-,且Na+进入阴极室,吸收液就可以再生。
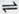 H2SO3 2H2SO3+O2
H2SO3 2H2SO3+O2 2H2SO4
2H2SO4(2)2OH-+ SO2=H2O+SO32-
(3)①酸性 HSO3-存在:HSO3-
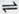 H++SO32-和HSO3-+H2O
H++SO32-和HSO3-+H2O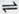 H2SO3+OH-,HSO3-的电离程度强于水解程度。 ②a b
H2SO3+OH-,HSO3-的电离程度强于水解程度。 ②a b(4)①HSO3-+H2O-2e-= SO42-+3H+
②H+在阴极得电子生成H2,溶液中c(H+)降低,促使HSO3-电离生成SO32-,且Na+进入阴极室,吸收液就可以再生。
试题分析:(1)SO2形成硫酸型酸雨时,二氧化硫和空气中的水、氧气反应得到硫酸:SO2+H2O
 H2SO3,2 H2SO3+O2
H2SO3,2 H2SO3+O2 2H2SO4;
2H2SO4;(2)二氧化硫被氢氧化钠溶液吸收制备亚硫酸钠溶液时:SO2+2OH- =SO32-+H2O;
(3)根据表中数据,可知,n(SO3²﹣):n(HSO3﹣)=1:91时,溶液的pH值为酸性,故NaHSO3溶液显酸性,在亚硫酸氢钠溶液中HSO3-存在:HSO3-
 SO32-+H+和HSO3-+H2O=H2SO3+OH-,HSO3-的电离程度强于水解程度,故溶液呈酸性。当吸收液呈中性时,溶液中的c(H+)=c(OH-),由于溶液中存在着电荷守恒,故c(Na+)+c(H+)=2c(SO32-)+ c(HSO3-)+c(OH-),可推出:c(Na+)=2c(SO32-)+c(HSO3-),a对;由于n(SO?²﹣):n(HSO?﹣)=1:1时,溶液的pH值为7.2,故中性时一定有c(HSO3-)> c(SO32-),可推出:c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-),b对;
SO32-+H+和HSO3-+H2O=H2SO3+OH-,HSO3-的电离程度强于水解程度,故溶液呈酸性。当吸收液呈中性时,溶液中的c(H+)=c(OH-),由于溶液中存在着电荷守恒,故c(Na+)+c(H+)=2c(SO32-)+ c(HSO3-)+c(OH-),可推出:c(Na+)=2c(SO32-)+c(HSO3-),a对;由于n(SO?²﹣):n(HSO?﹣)=1:1时,溶液的pH值为7.2,故中性时一定有c(HSO3-)> c(SO32-),可推出:c(Na+)> c(HSO3-)> c(SO32-)>c(H+)=c(OH-),b对;(4)根据电解槽所示的变化,可知HSO3-在阳极放电的电极反应式是:HSO3-+H2O-2e- =3H++SO42-;H+在阴极得电子生成H2,溶液中的c(H+)降低,促使HSO3-电离生成SO32-,且Na+进入阴极室,吸收液得以再生。
点评:本题综合性强,难度较大,主要考查学生分析解决问题的能力

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
 4Fe(OH)3 + 8OH-+ 3O2,
4Fe(OH)3 + 8OH-+ 3O2,
 2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为
2G(g)若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为 pC(g) + qD(g),当m、n、p、q为任意整数(不为零)时,能说明达到平衡状态的标志是( )
pC(g) + qD(g),当m、n、p、q为任意整数(不为零)时,能说明达到平衡状态的标志是( ) Br2(g)+H2(g)在密闭容器中进行,将密闭容器的体积缩小至原来的一半,下列说法正确的是( )
Br2(g)+H2(g)在密闭容器中进行,将密闭容器的体积缩小至原来的一半,下列说法正确的是( ) CH3OH(g).
CH3OH(g).