题目内容
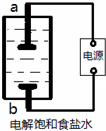 某兴趣小组模拟氯碱工业生产原理并探究其产品的性质.已知文献记载:
某兴趣小组模拟氯碱工业生产原理并探究其产品的性质.已知文献记载:①氯气与冷的氢氧化钠溶液反应生成NaClO;氯气与热的氢氧化钠溶液反应可生成NaClO和NaClO3.②在酸性较弱时KI只能被NaClO氧化,在酸性较强时亦能被NaClO3氧化.
(1)该小组利用如右图所示装置制取家用消毒液(主要成分为NaClO),a得到了氢气,则a为
阴极
阴极
(填“阳极”或“阴极”).生成NaClO的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O
Cl2+2OH-═Cl-+ClO-+H2O
.(2)该小组将0.784L(标准状况)Cl2通入50.00mL热的NaOH溶液中,两者恰好完全反应后,稀释到250.0mL.
①取稀释后的溶液25.00mL用醋酸酸化,加入过量KI溶液.用0.2000mol?L-1 Na2S2O3溶液滴定:I2+2S2O32-═2I-+S4O62-,消耗Na2S2O3溶液10.00mL时恰好到达终点.
②将上述滴定后的溶液用盐酸酸化至强酸性,再用上述Na2S2O3溶液滴定到终点,需Na2S2O3溶液30.00mL.
①操作②中氯酸钠与碘化钾反应的离子方程式为
ClO3-+6I-+6H+═3I2+Cl-+3H2O
ClO3-+6I-+6H+═3I2+Cl-+3H2O
.②反应后的溶液中次氯酸钠和氯酸钠的物质的量之比为
1:1
1:1
.③计算氢氧化钠溶液的物质的量浓度.
分析:(1)电解饱和食盐水,生成了氢气和氯气;a得到了氢气,溶液中产生了氢氧根,发生了还原反应,故A为阴极,生成NaClO的离子方程式是:Cl2+2OH-═Cl-+ClO-+H2O;
(2)①在酸性较强I-能被NaClO3氧化成碘单质,反应方程式是:ClO3-+6I-+6H+═3I2+Cl-+3H2O;
②根据反应方程找出关系式ClO-~2I-~I2~2S2O32-、ClO3-~6I-~3I2 ~6S2O32-,然后计算出次氯酸钠和氯酸钠的物质的量;
③根据氯原子守恒,n(Cl)=n(NaOH)计算出氢氧化钠的物质的量,溶液体积是0.05L,带入公式:c(NaOH)=
,求出氢氧化钠溶液中氢氧化钠的物质的量浓度.
(2)①在酸性较强I-能被NaClO3氧化成碘单质,反应方程式是:ClO3-+6I-+6H+═3I2+Cl-+3H2O;
②根据反应方程找出关系式ClO-~2I-~I2~2S2O32-、ClO3-~6I-~3I2 ~6S2O32-,然后计算出次氯酸钠和氯酸钠的物质的量;
③根据氯原子守恒,n(Cl)=n(NaOH)计算出氢氧化钠的物质的量,溶液体积是0.05L,带入公式:c(NaOH)=
| n(NaOH) |
| 0.05L |
解答:解:(1)a极生成了氢氧根,溶液中水电离的氢离子得到电子被还原,a为阴极,反应生成NaClO的离子方程式是:Cl2+2OH-═Cl-+ClO-+H2O;
故答案为:阴极;Cl2+2OH-═Cl-+ClO-+H2O;
(2)①酸性较强条件下,ClO3-将I-氧化成I2,根据化合价升降相等配平,反应的化学方程式是:ClO3-+6I-+6H+═3I2+Cl-+3H2O;
故答案为:ClO3-+6I-+6H+═3I2+Cl-+3H2O;
②用醋酸酸化,只有次氯酸钠氧化碘化钾,消耗Na2S2O3溶液10.00mL,根据关系式:ClO-~2I-~I2~2S2O32-
n(NaClO)=n(I2)=
×n(S2O32-)=
×0.2000mol/L×0.010L=0.001mol;
用盐酸酸化至强酸性,氯酸钾氧化碘化钠,消耗Na2S2O3溶液30.00mL;根据关系式:ClO3-~6I-~3I2 ~6S2O32-,
n(NaClO3)=
×n(I2)=
×n(S2O32-)=
×0.2000mol/L×0.03L=0.001mol;
故n(NaClO):n(NaClO3)=1:1;
故答案为:1:1;
③0.784L(标准状况)Cl2 的物质的量是:0.784 L÷22.4 L?mol-1=0.035mol;
根据关系式:Cl2~2NaOH,
1 2
n(NaOH)=2n(Cl2)=0.035mol×2=0.07mol,
c(NaOH)=
=1.4mol/L,
故答案为:c(NaOH)=1.4mol/L.
故答案为:阴极;Cl2+2OH-═Cl-+ClO-+H2O;
(2)①酸性较强条件下,ClO3-将I-氧化成I2,根据化合价升降相等配平,反应的化学方程式是:ClO3-+6I-+6H+═3I2+Cl-+3H2O;
故答案为:ClO3-+6I-+6H+═3I2+Cl-+3H2O;
②用醋酸酸化,只有次氯酸钠氧化碘化钾,消耗Na2S2O3溶液10.00mL,根据关系式:ClO-~2I-~I2~2S2O32-
n(NaClO)=n(I2)=
| 1 |
| 2 |
| 1 |
| 2 |
用盐酸酸化至强酸性,氯酸钾氧化碘化钠,消耗Na2S2O3溶液30.00mL;根据关系式:ClO3-~6I-~3I2 ~6S2O32-,
n(NaClO3)=
| 1 |
| 3 |
| 1 |
| 6 |
| 1 |
| 6 |
故n(NaClO):n(NaClO3)=1:1;
故答案为:1:1;
③0.784L(标准状况)Cl2 的物质的量是:0.784 L÷22.4 L?mol-1=0.035mol;
根据关系式:Cl2~2NaOH,
1 2
n(NaOH)=2n(Cl2)=0.035mol×2=0.07mol,
c(NaOH)=
| 0.07mol |
| 0.05L |
故答案为:c(NaOH)=1.4mol/L.
点评:本题考查了电极反应、次氯酸钠、氯酸钠的性质,涉及了较多的计算,成分考查了化学计算能力,可以找出关系式进行求解,本题难度中等.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
在常温下,某兴趣小组模拟“侯氏制碱法”制取碳酸钠,流程如下: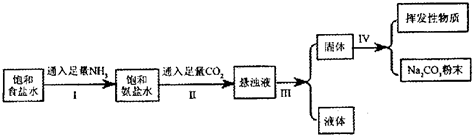
在常温下,有关物质的溶解度为:
(1)操作Ⅲ中的实验操作名称为 ;
(2)操作I和操作II总反应的离子方程式为 ;
(3)操作I和II不能颠倒的原因 ;
(4)检验所得的碳酸钠粉末是否含有NaHCO3,的实验方案是(写出操作步骤、现象、结论): ;
(5)为了测定所制取产物的纯度(假设杂质只有碳酸氢钠).该小组的实验步骤为:
i.使用下列装置组装实验装置,并检查气密性;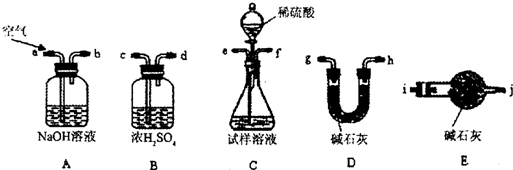
ii.称取Wg产品放入C装置的锥形瓶中,加适量蒸馏水溶解
iii.称量D装置的质量为W1g
iv.从分液漏斗滴入稀硫酸,直到不再产生气体为止
v.从a处缓缓鼓入一定量的空气,再次称量D装置质量为W2g.
vi.重复步骤v的操作,直到D装置的质量不再改变,称得D装置的质量为W3g.
根据上述实验回答如下问题:
①第i步,使用上述装置连接的接口顺序为:(b)→(e)(f)→ →
②产物中碳酸钠的质量分数为(数字可不必化简) .

在常温下,有关物质的溶解度为:
| 物质 | NH4Cl | NaHCO3 | Na2CO3 | NaCl |
| 溶解度/g | 37.2 | 9.6 | 21.5 | 36.0 |
(2)操作I和操作II总反应的离子方程式为
(3)操作I和II不能颠倒的原因
(4)检验所得的碳酸钠粉末是否含有NaHCO3,的实验方案是(写出操作步骤、现象、结论):
(5)为了测定所制取产物的纯度(假设杂质只有碳酸氢钠).该小组的实验步骤为:
i.使用下列装置组装实验装置,并检查气密性;

ii.称取Wg产品放入C装置的锥形瓶中,加适量蒸馏水溶解
iii.称量D装置的质量为W1g
iv.从分液漏斗滴入稀硫酸,直到不再产生气体为止
v.从a处缓缓鼓入一定量的空气,再次称量D装置质量为W2g.
vi.重复步骤v的操作,直到D装置的质量不再改变,称得D装置的质量为W3g.
根据上述实验回答如下问题:
①第i步,使用上述装置连接的接口顺序为:(b)→(e)(f)→
②产物中碳酸钠的质量分数为(数字可不必化简)
