题目内容
【题目】(13分)乙酸正丁酯是一种水果香味的无色透明液体,常用于调制香料和药物。实验室用正丁醇和乙酸制备,反应原理如下:
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
某兴趣小组拟用如图装置制备少量乙酸正丁酯:
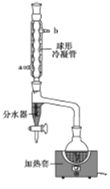
步骤1:加料。向干燥的100ml圆底烧瓶中加入37ml正丁醇、22ml冰醋酸及10滴浓硫酸(试剂加入顺序未确定),摇匀后,加入几粒沸石。然后安装分水器(先在分水器上端小心加水至分水器支管口处,然后再放出1~2ml的水)及回流冷凝管。
步骤2:加热回流。通过活塞控制分水器中水层液面的高度。反应完毕,停止加热。
步骤3:冷却(不可以拆卸回流冷凝管)。冷却至室温后,将烧瓶中的混合物与分水器中的酯层合并,转入分液漏斗中。
步骤4:依次用10ml水,10ml 10%碳酸钠溶液洗至中性(pH=7),再水洗一次,向洗涤后的有机相中加入适量的无水硫酸镁固体。放置一段时间后过滤、蒸馏、收集124~126℃馏分,得产品)
步骤5:用一干燥的小烧杯称产品,重量为29.0g。
相关物质的性质如下表:
物质名称 | 沸点/℃ | 熔点/℃ | 密度/g·cm-3 | 水中溶解度 |
正丁醇 | 117.3 | -89.5 | 0.80 | 7.1g/100g |
乙酸 | 118 | 16.6 | 1.0492 | 互溶 |
乙酸正丁酯 | 126.1 | -78 | 0.8826 | 1.4g/100g |
根据题意完成下列填空:
(1)加料时,三种试剂的加入顺序为 。
(2)该实验中,冷凝水从 (填“a”或“b”)口通入,使用分水器的目的是 。
(3)步骤2中判断反应结束的现象是 。
(4)步骤3中从分液漏斗中得到酯的操作 ,用10% Na2CO3溶液洗涤有机相,是为了除去有机相中的 (填结构简式)。
(5)步骤4中加入无水硫酸镁固体的作用是 。
(6)实验中正丁醇的转化率为 。
【答案】
(1)正丁醇、冰醋酸、浓硫酸
(2)a;及时分离出产物水,使化学平衡向生成酯的方向移动,提高酯的产率
(3)分离器中水层高度不再变化
(4)打开分液漏斗活塞,让水层从分液漏斗下口流出,酯层从上口倒出;H2SO4和CH3COOH
(5)除去有机相中残留的水
(6)65%
【解析】
试题分析:(1)向干燥的100ml圆底烧瓶中加入37ml正丁醇、22ml冰醋酸及10滴浓硫酸,由于浓硫酸稀释放热,加料时,应该后加浓硫酸,三种试剂的加入顺序可以为正丁醇、冰醋酸、浓硫酸,故答案为:正丁醇、冰醋酸、浓硫酸;
(2)冷凝水应该下进上出,因此从a口通入,使用分水器可以及时分离出产物水,使化学平衡向生成酯的方向移动,提高酯的产率,故答案为:a;及时分离出产物水,使化学平衡向生成酯的方向移动,提高酯的产率;
(3)反应结束分离器中水层高度不再变化,故答案为:分离器中水层高度不再变化;
(4)酯不溶于水,可以采用分液的操作分离,步骤3中从分液漏斗中得到酯的具体操作为打开分液漏斗活塞,让水层从分液漏斗下口流出,酯层从上口倒出;Na2CO3溶液能够与酯中的杂质H2SO4和CH3COOH反应,故答案为:打开分液漏斗活塞,让水层从分液漏斗下口流出,酯层从上口倒出;H2SO4和CH3COOH;
(5)无水硫酸镁可以除去有机相中残留的水,故答案为:除去有机相中残留的水;
(6)37mL正丁醇的质量为37mL×0.80g/mL=29.6g,22mL冰醋酸的质量为22mL×1.0492g/mL=23.0824g,设理论上29.6g正丁醇完全反应需乙酸的质量是y,则:
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
60g 74g
y 29.6g
y=![]() =24g>23.0824g,所以乙酸完全反应,按照乙酸计算乙酸正丁醇酯的理论质量,设乙酸正丁醇酯的理论质量为x,则:
=24g>23.0824g,所以乙酸完全反应,按照乙酸计算乙酸正丁醇酯的理论质量,设乙酸正丁醇酯的理论质量为x,则:
CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O
CH3COOCH2CH2CH2CH3+H2O
60g 116g
23.0824g x
所以x=![]() =44.626g,则乙酸正丁酯的产率为
=44.626g,则乙酸正丁酯的产率为![]() ×100%=65%,故答案为:65%
×100%=65%,故答案为:65%