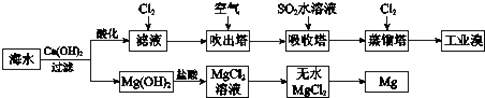
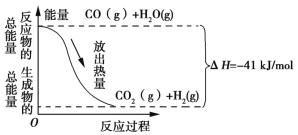
题目内容
【题目】用0.1molL﹣1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1molL﹣1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图: 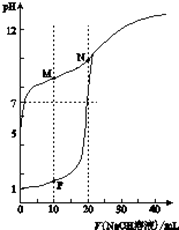
(1)HX为酸(填“强”或“弱”).
(2)N点pH>7的原因是(用化学用语表示) .
(3)下列说法正确的是(填字母).
a.M点c(HX)<c(X﹣)
b.M点c(Na+)>c(OH﹣)
c.P点c(Cl﹣)=0.05molL﹣1 .
【答案】
(1)弱
(2)X﹣+H2O?HX+OH﹣
(3)b
【解析】解:(1.)0.1molL﹣1 HCl溶液,是强酸溶液完全电离,所以溶液的PH=1;而0.1molL﹣1 HX溶液的PH>5说明是弱酸部分电离,所以答案是:弱;
(2.)N点pH>7的原因是因为两者等物质的量恰好完全反应生成强碱弱酸盐溶液水解呈碱性,所以水解反应方程式为:X﹣+H2OHX+OH﹣ , 所以答案是:X﹣+H2OHX+OH﹣;
(3.)a.M点生成等浓度的HX和NaX的混合溶液,溶液呈碱性,说明水解大于电离,所以M点c(HX)>c(X﹣),故错误;b.M点生成等浓度的HX和NaX的混合溶液,溶液呈碱性,说明水解大于电离,而水解程度微弱,所以M点c(Na+)>c(OH﹣),故正确;c.P点c(Cl﹣)= ![]() =0.067molL﹣1 , 故错误;故选:b.
=0.067molL﹣1 , 故错误;故选:b.

 口算题天天练系列答案
口算题天天练系列答案【题目】已知:I2+2S2O32﹣═S4O62﹣+2I﹣
相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10﹣20 | 2.6×10﹣39 | 1.7×10﹣7 | 1.3×10﹣12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3 , 为得到纯净的CuCl22H2O晶体,加入 , 调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)= . 过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl22H2O晶体.
(2)在空气中直接加热CuCl22H2O晶体得不到纯的无水CuCl2 , 原因是(用化学方程式表示).由CuCl22H2O晶体得到纯的无水CuCl2的合理方法是 .
(3)某学习小组用“间接碘量法”测定含有CuCl22H2O晶体的试样(不含能与I﹣发生反应的氧化性杂质)的纯度,过程如下:取0.36g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀.用0.100 0molL﹣1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL.
①可选用作滴定指示剂,滴定终点的现象是 .
②CuCl2溶液与KI反应的离子方程式为 .
③该试样中CuCl22H2O的质量百分数为