题目内容
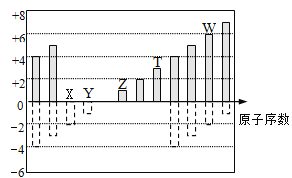
【题目】如图是部分短周期元素化合价与原子序数的关系,下列说法正确的是
A. 最高价氧化物对应水化物酸性: Y>W>T
B. 气态氢化物的稳定性: W>X
C. 单质还原性:T>Z
D. Z、T、W的最高价氧化物对应水化物可以相互反应
【答案】D
【解析】A、根据元素化合价的规律,图中没有正价的X与Y分别是O元素和F元素,所以Z、T、W依次为Na、Al、S元素。主要非金属性从强到弱顺序是F、O、S、Al,所以最高价氧化物对应的水化物酸性H2SO4>Al(OH)3,而F元素无最高正价,无对应的最高价氧化物的水化物,A错误。B、O的非金属性比S强,所以H2O比H2S稳定,B错误。C、Na的还原性比Al强,C错误。D、Z、T、W三种元素的最高价氧化物的水化物依次为NaOH、Al(OH)3、H2SO4,NaOH+Al(OH)3=NaAlO2+2H2O;H2SO4+2NaOH=Na2SO4+2H2O;2Al(OH)3+3H2SO4=Al2(SO4)3+6H2O。既它们可以相互反应,D正确

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】合成氨的反应为N2+3H2![]() 2NH3+Q。下表是某次反应时NH3的浓度变化:
2NH3+Q。下表是某次反应时NH3的浓度变化:
时间(min) | 0 | 5 | 10 | 15 | 20 |
c(NH3)(mol/L) | 0 | 0.30 | 0.44 | 0.50 | 0.50 |
完成下列填空:
(1)由表中数据计算0~10 min时,用H2表示的平均反应速率为________________。降低温度,反应的平衡常数将______________(填“增大”、“减小”或“不变”)。若要增大反应速率且提高H2利用率,可采取的措施有________________。
(2)若反应中气体混合物的密度保持不变,能否说明该反应已经达到平衡状态?并说明理由。____________________________________________________________________
(3)用右图所示装置进行有关氨气性质的实验,挤出胶头滴管中的水,打开止水夹后的实验现象是_____________。

(4)氨气溶于水后溶液显碱性的原因是(用方程式表示)____________________________________________。若在氨水中逐滴滴加盐酸,则溶液的pH将__________(填“增大”、“减小”或“不变”);当恰好完全反应时,则c(NH4+)________c(Cl-)(填“>”、“<”或“=”)。