题目内容
【题目】镓(Ga)、锗( Ge)、砷(As)、硒(Se)均为第四周期的元素,它们在高科技尖端科学特别是信息领域有着广泛的用途。试回答下列问题:
(1)基态锗原子的价电子排布图为_____。
(2)沸点:NH3_______AsH3(填“>”、“<”或“=”),原因是____________。
(3)H2SeO4和H2SeO3是硒的两种含氧酸,请根据结构与性质的关系,解释H2SeO4比H2SeO3 酸性强的原因________。
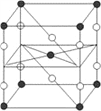
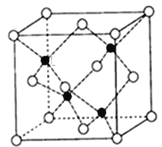
(4)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,同时得到一种最简单的有机物,写出该反应的方程式为_____;砷化镓的晶胞结构如下图所示,其晶胞边长为a pm(1pm=10-12m),则每立方厘米该晶体中所含砷元素的质量为_____g(用NA表示阿伏加德罗常数的值)。
【答案】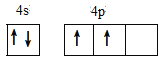 > NH3分子间存在氢键,所以NH3沸点高于AsH3 H2SeO4与H2SeO3比较前者非羟基氧多(或H2SeO3中的Se为+4价,而H2SeO4中的Se为+6价,导致Se-O-H中的O的电子更向Se偏移,越易电离出H+) (CH3)3Ga +AsH3
> NH3分子间存在氢键,所以NH3沸点高于AsH3 H2SeO4与H2SeO3比较前者非羟基氧多(或H2SeO3中的Se为+4价,而H2SeO4中的Se为+6价,导致Se-O-H中的O的电子更向Se偏移,越易电离出H+) (CH3)3Ga +AsH3![]() GaAs +3CH4
GaAs +3CH4 ![]()
【解析】
(1)锗是第四周期第ⅣA族元素,原子序数是32,所以依据核外电子排布规律可知,基态锗原子的价电子排布式为4s24p2,价电子排布图为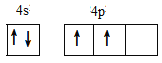 ,故答案为:
,故答案为: 。
。
(2)由于氮元素的非金属性强,因此NH3分子间存在氢键,所以NH3沸点高于AsH3沸点,故答案为:>;NH3分子间存在氢键,所以NH3沸点高于AsH3。
(3)由于H2SeO4和H3SeO3可表示为(HO)2SeO2和(HO)3Se,H2SeO4中非羟基氧多,H2SeO3中的Se为+4价,而H2SeO4中的Se为+6价,导致Se-O-H中的O的电子更向Se偏移,越易电离出H+,所以H2SeO4比H2SeO3酸性强,故答案为:H2SeO4与H2SeO3比较前者非羟基氧多(或H2SeO3中的Se为+4价,而H2SeO4中的Se为+6价,导致Se-O-H中的O的电子更向Se偏移,越易电离出H+)。
(4)砷化镓可由(CH3)2Ga和AsH3在700℃下反应制得,则根据原子守恒可知,另外一种生成物是甲烷,则该反应的方程式为(CH3)3Ga+AsH3![]() GaAs+3CH4;根据晶胞结构可知GaAs晶体中,每个As与4个Ga相连,且As原子全部在晶胞里面,共计是4个。晶胞边长为apm,所以晶胞的体积是a3pm3,所以每立方厘米含该晶胞的个数是
GaAs+3CH4;根据晶胞结构可知GaAs晶体中,每个As与4个Ga相连,且As原子全部在晶胞里面,共计是4个。晶胞边长为apm,所以晶胞的体积是a3pm3,所以每立方厘米含该晶胞的个数是![]() ,因此含有的As原子个数是
,因此含有的As原子个数是![]() ×4,物质的量是
×4,物质的量是![]() mol,所以As元素的质量是
mol,所以As元素的质量是![]() mol×75g/mol=
mol×75g/mol=![]() g,故答案为:(CH3)3Ga+AsH3
g,故答案为:(CH3)3Ga+AsH3![]() GaAs+3CH4;
GaAs+3CH4;![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列实验操作、现象、结论均完全正确的是( )
选项 | 操作 | 现象 | 结论 |
A | 在常温下测定Na2CO3和NaHCO3溶液的pH | Na2CO3溶液pH较大 | 水解能力:Na2CO3大于NaHCO3 |
B | 先向盛有1mL 0.1mol/L的AgNO3溶液的试管中滴加两滴0.1mol/L的NaCl溶液,再向其中滴加0.1mol/L的NaI溶液。 | 滴加NaCl溶液有白色沉淀生成,滴加NaI溶液后有黄色沉淀生成 | AgCl沉淀可转化成AgI沉淀 |
C | 电解饱和CuCl2溶液实验中,用润湿的淀粉—碘化钾试纸靠近阳极 | 润湿的淀粉—碘化钾试纸变蓝 | 阳极产生Cl2 |
D | 饱和FeCl3溶液中加入少量NaCl固体 | 溶液颜色变浅 | 加入NaCl固体后,FeCl3的水解平衡逆向移动 |
A. AB. BC. CD. D
【题目】下表是实验室制备气体的有关内容:
编号 | 实验内容 | 实验原理 |
① | 制氧气 | H2O2→O2 |
② | 制氨气 | NH4Cl→NH3 |
③ | 制氯气 | HCl→Cl2 |
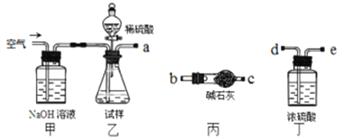
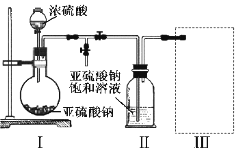
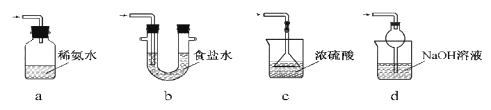
(1)上述气体中:从制备过程看,必须选择合适的氧化剂才能实现的是_________(填气体的化学式,下同);从反应中有无电子转移的角度看,明显不同于其他气体的是______,写出实验室制取该气体的化学方程式_______________________________
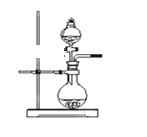
(2)若用上述装置制备NH3,则选择的试剂为____________________。
(3)制备Cl2需用8 mol/L的盐酸100mL,现用12 mol/L的盐酸来配制。
①需要12 mol/L的盐酸的体积为__________mL(精确到0.1 mL)
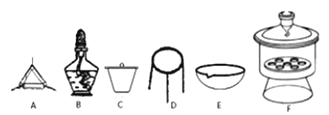
②在容量瓶的使用方法中,下列操作不正确的是_______________(填写标号)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时用量筒量取浓盐酸后用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平
D.定容后盖好瓶塞,用食指顶住,用另一只手手指托住瓶底,把容量瓶倒转和摇动多次