题目内容
【题目】2016年10月11日,神舟十一号飞船搭乘CZ﹣2F火箭成功发射。在重达495 吨的起飞重量中,95%的都是化学推进剂。
(1)降冰片烯![]() (C7H10)是一种重要的高密度液体燃料化学推进剂。已知:
(C7H10)是一种重要的高密度液体燃料化学推进剂。已知:
燃料 | 密度(gcm-3) | 体积热值(JL-1) |
降冰片烯 | 1.0 | 4.2×107 |
写出表示降冰片烯标准燃烧热的热化学方程式:_____。
(2)CH3OH和液氧是常用的液体火箭推进剂。
①已知:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(l)△H1
CH3OH(g)+H2O(l)△H1
2H2(g)+O2(l)=2H2O(l)△H2
CH3OH(g)=CH3OH(l)△H3
2CH3OH(l)+3O2(l)=2CO2(g)+4H2O(l)△H4
则△H4=_____(用△H1、△H2、△H3来表示)。
②某温度下,发生反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。在体积为2L的密闭容器中加入1mol CH3OH和1mol H2O,第4min达到平衡,容器内c(CO2)随时间的变化情况如图1所示,求此反应在该温度下的平衡常数_____。保持其它条件不变,在第5min时向体系中再充入0.2mol CO2和0.4mol H2,第8min重新达到平衡,此时c(H2)=c(CH3OH)。请在图中画出5到9min的c(CO2)变化曲线示意图。
CH3OH(g)+H2O(g)。在体积为2L的密闭容器中加入1mol CH3OH和1mol H2O,第4min达到平衡,容器内c(CO2)随时间的变化情况如图1所示,求此反应在该温度下的平衡常数_____。保持其它条件不变,在第5min时向体系中再充入0.2mol CO2和0.4mol H2,第8min重新达到平衡,此时c(H2)=c(CH3OH)。请在图中画出5到9min的c(CO2)变化曲线示意图。
(3)NH4NO3也是一种重要的固体推进剂,可通过电解NO制备NH4NO3,其工作原理如图2所示,A电极的名称为_____极,请写出在B电极上发生的电极反应式:_____。

【答案】 C7H10(l)+9.5O2(g)=7CO2(g)+5H2O(l)△H=-3948kJ/mol 3△H2-2△H1-2△H3 59.26 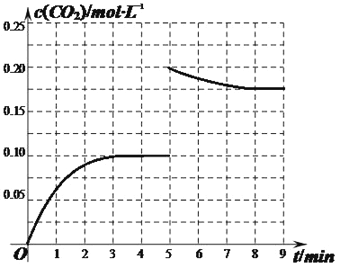 NO-3e-+2H2O=NO3-+4H+
NO-3e-+2H2O=NO3-+4H+
【解析】(1)C7H10的摩尔质量为94g/mol,故燃烧1mol降冰片烯标准燃烧热为△H=-(4.2×107J/L×94g/mol÷1000g/L)=-3948kJ/mol,故热化学方程式为C7H10(l)+9.5O2(g)=7CO2(g)+5H2O(l)①△H=-3948kJ/mol;(2)已知:
ⅰ、CO2(g)+3H2(g)![]() CH3OH(g)+H2O(l)△H1
CH3OH(g)+H2O(l)△H1
ⅱ、2H2(g)+O2(l)═2H2O(l)△H2
ⅲ、CH3OH(g)═CH3OH(l)△H3
根据盖斯定律可知3×ⅱ﹣2×ⅰ﹣2×ⅲ即得到2CH3OH(l)+3O2(l)═2CO2(g)+4H2O(l)的△H4=3△H2﹣2△H1﹣2△H3;
② CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
起始浓度(mol/L)0 0 0.5 0.5
变化浓度(mol/L)0.1 0.3 0.1 0.1
平衡浓度(mol/L)0.1 0.3 0.4 0.4
所以k=0.4×0.4/0.2×0.33=59.26;反应物浓度增大,使平衡不断向正反应方向进行,因此图像为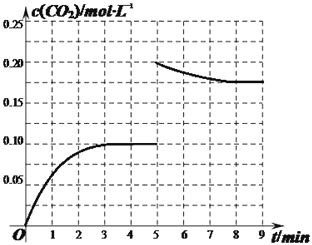 ;(3)由图可知,A极上NO生成NH4+,发生还原反应,为电解池阴极;B极上NO生成NO3﹣,发生氧化反应,故电极反应方程式为NO-3e-+2H2O=NO3-+4H+。
;(3)由图可知,A极上NO生成NH4+,发生还原反应,为电解池阴极;B极上NO生成NO3﹣,发生氧化反应,故电极反应方程式为NO-3e-+2H2O=NO3-+4H+。

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案【题目】某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50mol/L NaOH溶液

(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体___g。
(2)从表中选择称量NaOH固体所需要的仪器是(填字母):___。
名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
仪器 |
|
|
|
|
|
|
序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(1)写出该反应的热化学方程式(中和热为57.3kJ/mol):___。
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表:
①请填写下表中的空白:
| 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ________ |
2 | 27.0 | 27.4 | 27.2 | 31.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.3 | |
②近似认为0.50mol/L NaOH溶液和0.50mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18J/(g℃)。则中和热△H=___(取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)___。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度