题目内容
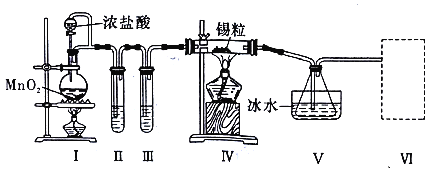
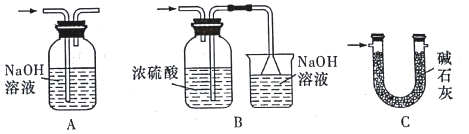
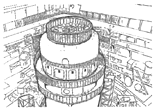
【题目】有关物质的转化关系如下图所示(部分生成物和反应条件已略去)。A为由两种元素组成的固体,含非金属质量分数为39.13%;D、E、L均为无色气体,E和L难溶于水;F为常见金属;G、I、J焰色反应显黄色;M为有颜色的固体。

请回答下列问题:
(1)E的化学式为___________________。
(2)G的电子式为___________________。
(3)写出反应①的化学方程式:_______________________________。
(4)写出反应②的离子方程式:_______________________________。
【答案】 NO ![]() FeC3+8HNO3=Fe(NO3)3+3CO2↑+5NO↑+4H2O 2Fe3++3CO32-+3H2O==2Fe(OH)3↓+3CO2↑
FeC3+8HNO3=Fe(NO3)3+3CO2↑+5NO↑+4H2O 2Fe3++3CO32-+3H2O==2Fe(OH)3↓+3CO2↑
【解析】G、I、J焰色反应显黄色,含有钠元素,D、E、L均为无色气体,E和L难溶于水,因此G可能是过氧化钠,D是二氧化碳,I是氢氧化钠,L是氧气,E是NO,B是硝酸,M为有颜色的固体,M可能是氢氧化铁,F为常见金属,则F是铁,C是硝酸铁,H是硝酸亚铁,A为由两种元素组成的固体,含非金属质量分数为39.13%,A是由C和Fe两种元素形成的,原子数之比是![]() ,因此A的化学式为FeC3。
,因此A的化学式为FeC3。
(1)E的化学式为NO。(2)过氧化钠的电子式为![]() 。(3)根据以上分析可知反应①的化学方程式为FeC3+8HNO3=Fe(NO3)3+3CO2↑+5NO↑+4H2O。(4)反应②的离子方程式为2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑。
。(3)根据以上分析可知反应①的化学方程式为FeC3+8HNO3=Fe(NO3)3+3CO2↑+5NO↑+4H2O。(4)反应②的离子方程式为2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑。

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D