题目内容
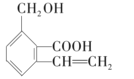
【题目】通过测定混合气中![]() 含量可计算已变质的
含量可计算已变质的![]() 含
含![]() 纯度,实验装置如图
纯度,实验装置如图![]() 为弹性良好的气囊
为弹性良好的气囊![]() ,下列分析错误的是
,下列分析错误的是![]()
![]()
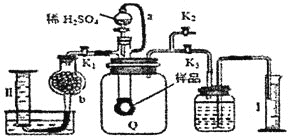
A.干燥管b中装入碱石灰
B.测定气体总体积必须关闭![]() 、
、![]() ,打开
,打开![]()
C.测定总体积后,关闭![]() ,打开
,打开![]() ,可观察到Q气球慢慢缩小,并测出氧气体积
,可观察到Q气球慢慢缩小,并测出氧气体积
D.Q气球中产生的气体主要成份![]() 、
、![]()
【答案】C
【解析】
本题考查混合物含量的测定,题目难度中等,本题要搞清量筒Ⅰ、Ⅱ的作用,根据反应的化学方程式计算即可解答。
A.加入稀硫酸与样品反应,在Q气球中得到二氧化碳和氧气,用碱石灰吸收二氧化碳和水蒸气,在量筒Ⅱ中排水法测氧气的量,进而计算过氧化钠的量,故A正确;
B.反应产生的![]() 、
、![]() 使气球变大,将广口瓶中气体排出,水进入量筒Ⅰ中,所以量筒Ⅰ中水的体积即为产生的
使气球变大,将广口瓶中气体排出,水进入量筒Ⅰ中,所以量筒Ⅰ中水的体积即为产生的![]() 、
、![]() 的总体积,所以滴稀
的总体积,所以滴稀![]() 前必须关闭
前必须关闭![]() 、
、![]() 打开
打开![]() ,故B正确;
,故B正确;
C.读取气体总体积后关闭![]() 缓缓打开
缓缓打开![]() 还要打开
还要打开![]() ,才能观察到Q气球慢慢缩小,原因是不打开
,才能观察到Q气球慢慢缩小,原因是不打开![]() 体系是密闭的,气球体积无法减小,故C错误;
体系是密闭的,气球体积无法减小,故C错误;
D.加入酸后Q内发生反应:![]() ;
;![]() ,反应产生
,反应产生![]() 、
、![]() 气体,故D正确。
气体,故D正确。
故选C。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(1)ClO2的制备:
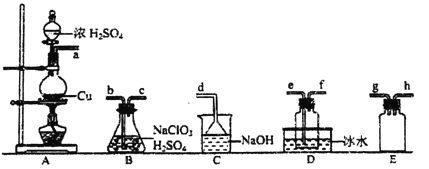
已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4
①装置A中反应的化学方程式为__________。
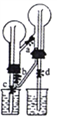
②欲收集ClO2,选择上图中的装置,其连接顺序为a→__________(按气流方向,用小写字母表示)。
③装置D的作用是___________________。
(2)C1O2与Na2S的反应

将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究I中反应的产物。
操作步骤 | 实验现象 | 结论 |
取少量I中溶液于试管甲中,滴加品红溶液和盐酸。 | 品红始终不褪色 | ①无_________生成 |
另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ②____________ | 有SO42-生成 |
③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙中,_______。 | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S的反应的离子方程式为______________,用于处理含硫废水时,ClO2相对于Cl2的优点是_________________(任写一条)。
【题目】现有7瓶失去标签的试剂瓶,已知它们盛装的液体可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖溶液、蔗糖溶液。现通过如下实验来确定各试剂中所装液体的名称。
实验步骤和方法 | 实验现象 |
①把7瓶液体依次标号为A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
③分别取少量7种液体于试管中加新制的 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
④各取C、D、E少量于试管中,加稀 | 只有C中仍有分层现象,且在D的试管中闻到特殊香味 |
试写出下列序号代表的液体名称:
A___________________,B___________________,C___________________,D___________________,E___________________,F___________________,G___________________。