题目内容
【题目】25℃和101kPa时,甲烷、乙炔和乙烯组成的混合烃10mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小17.5mL,原混合烃中乙炔的体积分数为( )
A.12.5%
B.25%
C.50%
D.75%
【答案】C
【解析】解:除去水蒸气,恢复到原来的温度和压强,则:
CH4+ | 2O2 | = | CO2+ | 2H2O | △V |
1 | 2 | 1 | 2 |
C2H4+ | 3O2 | = | 2CO2+ | 2H2O | △V |
1 | 3 | 2 | 2 |
C2H2+ |
| = | 2CO2+ | H2O | △V |
1 | 2.5 | 2 | 1.5 |
CH4和C2H4反应后体积缩小的量是相同的,故可将两者看成是一种物质,
设CH4和C2H4一共为xmL,C2H2为ymL,则:![]()
解之得x=5,y=5,
则原混合烃中乙炔的体积分数为 ![]() ×100%=50%,
×100%=50%,
故选C.

【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= .
(2)从表中看出,升高温度,K值 , 则CO2的转化率 , 化学反应速率 . (以上均填“增大”“减小”或“不变”)
(3)能判断该反应是否达到化学平衡状态的依据是
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(H2)=c(CO)c(H2O),试判断此时的温度为℃.
【题目】某学生欲通过实验方法验证Fe2+的性质.
(1)该同学在实验前,依据Fe2+的性,填写了下表.
实验操作 | 预期现象 | 反应的离子方程式 |
向盛有新制FeSO4溶液的试管中滴入数滴浓硝酸,振荡 | 试管中产生红棕色气体,溶液颜色逐渐变黄 | Fe2++NO |
依照表中操作,该同学进行实验.观察到液面上方气体逐渐变为红棕色,但试管中溶液颜色却变为深棕色.
(2)为了进一步探究溶液变成深棕色的原因,该同学进行如下实验.向原新制FeSO4溶液和反应后溶液中均加入KSCN溶液,前者不变红色,后者(加了数滴浓硝酸的FeSO4溶液)变红.该现象的结论是 .
(3)该同学通过查阅资料,认为溶液的深棕色可能是NO2或NO与溶液中Fe2+或Fe3+发生反应而得到的.为此他利用如图装置(气密性已检验,尾气处理装置略)进行探究.ⅰ.打开活塞a、关闭b,并使甲装置中反应开始后,观察到丙中溶液逐渐变为深棕色,而丁中溶液无明显变化.
ⅱ.打开活塞b、关闭a,一段时间后再停止甲中反应.
ⅲ.为与ⅰ中实验进行对照,更换丙、丁后(溶质不变),使甲中反应继续,观察到的现象与步骤ⅰ中相同.
①铜与足量浓硝酸反应的化学方程式是;
②装置乙的作用是;
③步骤ⅱ的目的是;
④该实验可得出的结论是 .
(4)该同学重新进行(1)中实验,观察到了预期现象,其实验操作是 .
【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示.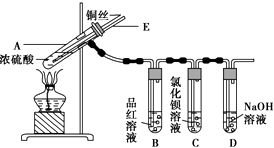
实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面.
请回答下列问题:
(1)A试管中发生反应的化学方程式为 .
(2)能够证明铜与浓硫酸反应生成气体的实验现象是 .
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置.
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 |
写出其中SO2表现还原性的离子反应方程式: .
(4)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是 .
(5)实验完毕后,装置中残留的气体有毒,不能打开导管上的胶塞.为了防止该气体排入空气中污染环境,拆除装置前,应当采取的操作是 .
(6)将SO2气体通入含有n mol Na2S的溶液中,充分反应后,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体mol(不考虑溶解的SO2).