题目内容
在4 L密闭容器中充入6 mol A气体和5 mol B气体,在一定条件下发生反应:
3A(g) + B(g) 2C(g) + xD(g) ,若平衡时生成了2 mol C,D的浓度为0.5 mol·L-1,下列判断正确的是( )
2C(g) + xD(g) ,若平衡时生成了2 mol C,D的浓度为0.5 mol·L-1,下列判断正确的是( )
3A(g) + B(g)
 2C(g) + xD(g) ,若平衡时生成了2 mol C,D的浓度为0.5 mol·L-1,下列判断正确的是( )
2C(g) + xD(g) ,若平衡时生成了2 mol C,D的浓度为0.5 mol·L-1,下列判断正确的是( )| A.X=2 |
| B.平衡时混合气体密度增大 |
| C.平衡时B的浓度为1.5 mol·L-1 |
| D.当A与B的正反应速率为3:1时该反应达到平衡 |
A
试题分析:达到平衡时,生成了2molC,D的物质的量为4L×0.5mol/L=2mol,
3A(g)+B(g)
 2C(g)+xD(g)
2C(g)+xD(g)起始:6mol 5mol 0 0
转化:3mol 1mol 2mol xmol
平衡:3mol 4mol 2mol 2mol
△n(D)=0.5mol/L×4L=2mol,平衡时生成2molC,故2:x=2mol:2mol,解得x=2,故A正确;
反应体系中各组分都是气体,混合气体的质量不变,容器的容积恒定,根据ρ=m/V可知混合气体的密度不变,故B错误;C、平衡时B的浓度为4 mol /4 L=1mol·L-1;D、此反应无论何时A与B的正反应速率均为3:1。

练习册系列答案
相关题目
 A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是 N2(g)+3H2(g) △H=+92.4kJ/mol
N2(g)+3H2(g) △H=+92.4kJ/mol I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化如图示曲线。下列说法正确的是
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化如图示曲线。下列说法正确的是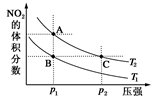
 pC(g)+qD(g) △H<0。下列结论中错误的是( )
pC(g)+qD(g) △H<0。下列结论中错误的是( ) CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示:
CH3OH(g) + H2O(g) △H =" -49.0" kJ/mol。测得CO2和CH3OH(g)的浓度随时间变化如图所示: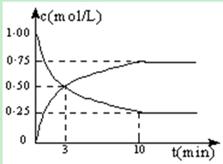
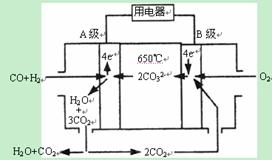
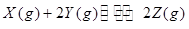 、②
、② 分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示:
分别在密闭容器的两个反应室中进行,反应室之间有无摩擦、可滑动的密闭隔板。反应开始和达到平衡状态时有关物理量的变化如图所示: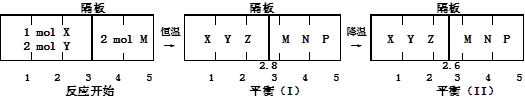
 CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表: