题目内容
水的电离平衡曲线如图所示,下列说法正确的是
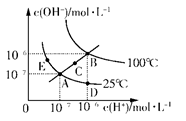

| A.图中五点KW间的关系:B>C>A=D=E |
| B.若从A点到D点,可采用在水中加入少量酸的方法 |
| C.若从A点到C点,可采用温度不变时在水中加入适量NaOH固体的方法 |
| D.若处在B点时,将pH=2的硫酸与pH=12的KOH等体积混合后,溶液显中性 |
AB
试题分析:A.在图中可看出:A、D、E是在25 ℃水的电离平衡曲线;三种物质的Kw相同;B是在100℃水的电离平衡曲线产生的离子浓度的关系;C在A、B的连线上,由于水是弱电解质,升高温度,促进水的电离,水的离子积常数增大则图中五点KW间的关系:B>C>A=D=E。正确。B.若从A点到D点,由于温度不变,溶液中c(H+)增大,c(OH-)减小。可采用在水中加入少量酸的方法。正确。C.若从A点到C点,由于水的离子积常数增大,所以可采用升高温度的方法。错误。D.若处在B点时,由于Kw=10—12。 pH=2的硫酸,c(H+)=10-2mol/L, pH=12的KOH, c(OH-)=1mol/L,若二者等体积混合,由于n(OH-)> n(H+),所以溶液显碱性。错误。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目

 2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( )
2SO3(g)在一个体积不变的密闭容器中反应,达到平衡状态的标志是( ) 2C,达到化学反应限度时,B的物质的量可能是( )
2C,达到化学反应限度时,B的物质的量可能是( ) 2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是
2C(气),平衡时C的体积分数与温度和压强的关系如图所示,下列判断正确的是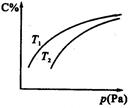
 2SO3(g).某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
2SO3(g).某温度下,将2mol SO2和1mol O2置于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是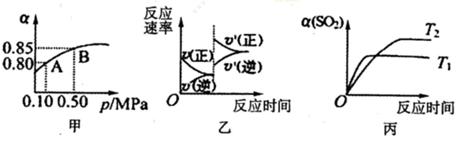
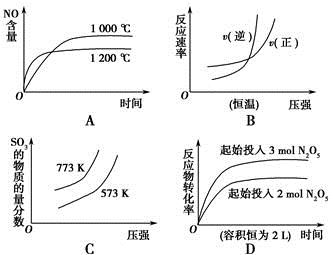
 4NO(g)+6H2O(g)ΔH=-a kJ·mol-1
4NO(g)+6H2O(g)ΔH=-a kJ·mol-1 4NO2(g)+O2(g) ΔH=+d kJ·mol-1
4NO2(g)+O2(g) ΔH=+d kJ·mol-1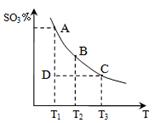
 2SO3(g)的△H____0(填“>”或“<”),若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”、“向右”或“不移动”);
2SO3(g)的△H____0(填“>”或“<”),若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡 移动(填“向左”、“向右”或“不移动”); 2CO2+N2。它的优点是 ;
2CO2+N2。它的优点是 ;
 CO2(g)+H2(g),有如下数据:
CO2(g)+H2(g),有如下数据: