题目内容
【题目】下列指定反应的离子方程式书写正确的是( )
A.将浓FeCl3溶液加入沸水中:Fe3++3H2O=Fe(OH)3↓+3H+
B.用氨水吸收足量的SO2气体:NH3·H2O+SO2=NH![]() +HSO
+HSO![]()
C.向NH4HSO4溶液中加入足量Ba(OH)2溶液:Ba2++OH-+H++SO![]() =BaSO4↓+H2O
=BaSO4↓+H2O
D.用稀氢碘酸溶液除去铁制品表面的铁锈:Fe2O3+6H+=2Fe3++3H2O
【答案】B
【解析】
A.将浓FeCl3溶液加入沸水中生成Fe(OH)3胶体而不是沉淀,正确离子方程式为Fe3++3H2O![]() Fe(OH)3(胶体)+3H+,故A错误;
Fe(OH)3(胶体)+3H+,故A错误;
B.氨水吸收足量的SO2气体生成亚硫酸氢铵,离子方程式为NH3·H2O+SO2=NH![]() +HSO
+HSO![]() ,故B正确;
,故B正确;
C.向NH4HSO4溶液中加入足量Ba(OH)2溶液,铵根也会和氢氧根反应,正确离子方程式为NH4++H++SO42-+Ba2++2OH-=BaSO4↓+H2O+NH3·H2O,故C错误;
D.铁离子会将碘离子氧化成碘单质,正确离子方程式为2I-+Fe2O3+6H+=2Fe2++3H2O+I2,故D错误;
故答案为B。

 阅读快车系列答案
阅读快车系列答案【题目】市售一次性电池品种很多的,碱性锌锰电池的日常生活中用量很大。回收废旧锌锰电池并进行重新处理,可以获得MnO2及其他副产品,其工艺流程如下:
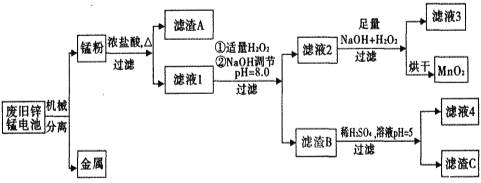
已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含量有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表。
物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2/Mn(OH)3 |
开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
完全沉淀pH (c≤1.0x10-5mol/L) | 3.7 | 9.6 | 8.0 | 8.8 |
(1)加入NaOH溶液调节pH=8.0,目的是___。计算常温下Zn(OH)2的溶度积常数Ksp[Zn(OH)2]=___。
(2)写出滤液2中的Mn2+变成MnO2的离子方程式___。
(3)写出滤渣B与稀硫酸在pH=5时的化学方程式___。
(4)工艺中还可以将滤液4进行___、___、___、___、洗涤得到含结晶水的硫酸盐晶体。
(5)MnO2常用来制取KMnO4,在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液的总反应方程式___。
【题目】下列有关实验操作与相应结论都正确的是![]()
选项 | 实验操作及现象 | 实验结论 |
A | 取少量硫酸亚铁铵晶体放入试管,加浓NaOH溶液,加热,试管口湿润蓝色石蕊试纸变红. | 可证明晶体的成分中含有 |
B | Z、W两试管中分别盛有pH和体积相同的盐酸和醋酸溶液,同时分别投入质量大小、形状相同的少量锌粒,Z中产生气体速率快 | Z中盛放的是醋酸 |
C | 向尿液中加入新制 | 说明尿液中不含有葡萄糖 |
D | 某待测液先滴入氯水无明显现象,后滴入硫氰化钾溶液出现血红色 | 该待测液中一定含有 |
A.AB.BC.CD.D
【题目】现有7瓶失去标签的试剂瓶,已知它们盛装的是有机液体,可能是乙醇、乙酸、苯、乙酸乙酯、油脂、葡萄糖溶液、蔗糖溶液。现通过如下实验来确定各试剂瓶中所装液体的名称。已知:乙酸乙酯在稀![]() 溶液中发生水解反应的化学方程式为
溶液中发生水解反应的化学方程式为![]() 。
。
实验步骤和方法 | 实验现象 |
①把7瓶液体依次标号为A、B、C、D、E、F、G后闻气味 | 只有F、G两种液体没有气味 |
②各取少量于试管中加水稀释 | 只有C、D、E三种液体不溶解而浮在水上层 |
③分别取少量7种液体于试管中加新制的 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
④各取C、D、E少量于试管中,加稀 | 只有C中仍有分层现象,且在D的试管中闻到特殊香味 |
试写出下列标号代表的液体名称:
A_______,B_______,C_______,D_______,E_______,F_______,G_______。