题目内容
【题目】利用下图所示装置模拟工业NaClO3与Na2SO3在浓H2SO4存在下制备ClO2,并以ClO2为原料制备NaClO2(已知:高于60℃时,NaClO2分解生成NaClO3和NaCl)。
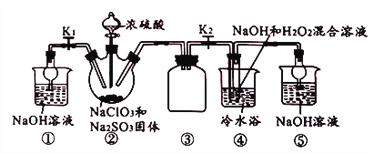
下列说法不正确的是( )
A. 逐滴加入浓硫酸可提高ClO2的利用率
B. 装置④中所得产物中可能含有Na2SO4杂质
C. 从装置④反应后的溶液中获得晶体,可采用常压蒸发结晶
D. 制备NaClO2结束时,应关闭分液漏斗活塞,打开K1,关闭K2
【答案】C
【解析】逐滴加入浓硫酸可以控制生成ClO2的速率,使ClO2与氢氧化钠、双氧水充分反应,提高ClO2的利用率,故A正确;装置②中能生成少量的SO2,SO2与氢氧化钠、双氧水反应生成Na2SO4,故B正确;高于60℃时,NaClO2分解生成NaClO3和NaCl,若采用常压蒸发结晶,NaClO2易发生分解反应,故C错误;制备NaClO2结束时,应关闭分液漏斗活塞,打开K1,关闭K2,用①中氢氧化钠溶液吸收尾气,故D正确。

练习册系列答案
相关题目
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )

选项 物质 | a | b | c |
A | Al | AlCl3 | Al(OH)3 |
B | HNO3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | S | SO2 | H2SO4 |
A. A B. B C. C D. D