题目内容
【题目】已知A是来自石油的重要有机化工原料,其产量用来衡量一个国家石油化工发展水平,E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。
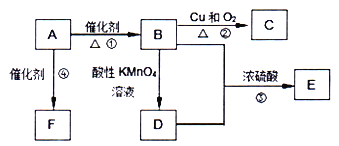
(1)A、D分子中的官能团分别名称为_______、_______。
(2)反应①的反应类型为________。
(3)反应②的化学方程式为_________。
(4)反应③的化学方程式为_______;该反应的反应类型为_____。
(5)反应④的化学方程式为_______。
【答案】 碳碳双键 羧基 加成反应 2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O CH3COOH+CH3CH2OH
2CH3CHO + 2H2O CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O 酯化反应或取代反应 nCH2=CH2
CH3COOCH2CH3+H2O 酯化反应或取代反应 nCH2=CH2![]()
![]()
【解析】A是来自石油的重要有机化工原料,产量可以用来衡量一个国家石油化工发展水平,可知A是H2C=CH2,E是具有果香味的有机物,E是酯,酸和醇反应生成酯,则B和D一种是酸一种是醇,B能被氧化生成D,A反应生成B,碳原子个数不变,则B是CH3CH2OH,D是CH3COOH,铜作催化剂、加热条件下,CH3CH2OH被氧气氧化生成C,所以C是CH3CHO,乙酸与乙醇分子酯化反应生成E为CH3COOCH2CH3,A反应生成F,F是一种高聚物,乙烯发生加聚反应生成高聚物F为![]()
(1)A、D分子中的官能团分别名称为碳碳双键、羧基。(2)H2C=CH2与水反应生成乙醇,反应①的反应类型为加成反应。(3)反应②的化学方程式为2CH3CH2OH + O2 ![]() 2CH3CHO + 2H2O 。(4)反应③的化学方程式为 CH3COOH+CH3CH2OH
2CH3CHO + 2H2O 。(4)反应③的化学方程式为 CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O ;该反应的反应类型为酯化反应或取代反应 。(5)反应④的化学方程式为nCH2=CH2
CH3COOCH2CH3+H2O ;该反应的反应类型为酯化反应或取代反应 。(5)反应④的化学方程式为nCH2=CH2![]()
![]() 。
。

【题目】水能灭火也可以引火.把少量过氧化钠(Na2O2)粉末用干燥脱脂棉包裹(脱脂棉和过氧化钠不反应),将少量水滴到包有过氧化钠的脱脂棉上,则脱脂棉迅速发生燃烧.小明对此现象很感兴趣,于是他和同学们进行如下探究:
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】
①可能有一种气体和另一种物质生成.
②反应过程中可能有能量变化.
【设计实验】如图所示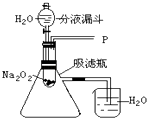
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中的分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是 . 发生的反应方程式为其中氧化剂为;还原剂为;产生0.2mol的氧气,需要的转移电子mol.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因: .
(3)实验二:继续探究反应后生成的另一种物质是什么?
小强猜想另一种物质是Na2CO3 , 小明认为不可能,小明的依据是 .
(4)为了证实小明的看法,请你设计一个证明CO32﹣不存在的实验.
实验步骤 | 实验现象 | 实验结论 |
(5)小明取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的另一种物质是(填化学式).
