题目内容
【题目】已知:2CrO42﹣+2H+Cr2O72﹣+H2O.25℃时,调节初始浓度为1.0molL﹣1 的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72﹣)和c(H+),获得如图所示的曲线.下列说法不正确的是( ) 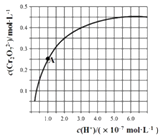
A.平衡时,pH越小,c(Cr2O72﹣)越大
B.A点CrO42﹣的平衡转化率为50%
C.A点CrO42﹣转化为Cr2O72﹣反应的平衡常数K=1014
D.平衡时,若溶液中c(Cr2O72﹣)=c(Cr2O42﹣),则c(H+)>2.0×10﹣7 molL﹣1
【答案】D
【解析】解:A、由图可知氢离子浓度越大,c(Cr2O72﹣)越大,所以pH越小,c(Cr2O72﹣)越大,故A正确;
B、由图可知A点时Cr2O72﹣的平衡浓度为0.25mol/L,所以转化的CrO42﹣的浓度为:0.5mol/L,则A点CrO42﹣的平衡转化率为50%,故B正确;
C、2CrO42﹣+2H+Cr2O72﹣+H2O的平衡常数为:K= ![]() =
= ![]() =1014 , 故C正确;
=1014 , 故C正确;
D、平衡时,若溶液中c(Cr2O72﹣)=c(CrO42﹣),而2c(Cr2O72﹣)+c(CrO42﹣)=1.0molL﹣1 , 所以c(Cr2O72﹣)= ![]() molL﹣1 , 而图中c(Cr2O72﹣)=0.35mol/L时,对应氢离子的浓度为2.0×10﹣7 molL﹣1 , 则溶液中c(Cr2O72﹣)=c(Cr2O42﹣),则c(H+)<2.0×10﹣7 molL﹣1 , 故D错误;
molL﹣1 , 而图中c(Cr2O72﹣)=0.35mol/L时,对应氢离子的浓度为2.0×10﹣7 molL﹣1 , 则溶液中c(Cr2O72﹣)=c(Cr2O42﹣),则c(H+)<2.0×10﹣7 molL﹣1 , 故D错误;
故选D.

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3 , 其流程如下: 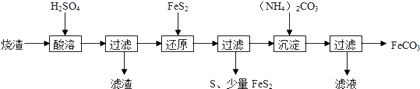
已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
FeS2+14Fe3++8H2O=15Fe2++2SO42﹣+16H+
(1)加入FeS2还原后,检验Fe3+是否反应完全的试剂为 .
(2)所得FeCO3需充分洗涤,检验是否洗净的方法是 . “沉淀”时,pH不宜过高,否则制备的FeCO3中可能混有的杂质是 .
(3)①写出“还原”时反应Ⅱ的离子方程式: .
(4)②“还原”前后溶液中部分离子的浓度见下表(溶液体积变化或略不计):
离子 | 离子浓度(molL﹣1) | |
还原前 | 还原后 | |
Fe2+ | 0.10 | 2.5 |
SO42﹣ | 3.5 | 3.7 |
请计算反应Ⅰ、Ⅱ中被还原的Fe3+的物质的量之比(写出计算过程).
【题目】随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.
完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化.(选填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/molL﹣1 | [H2]/molL﹣1 | [CH4]/molL﹣1 | [H2O]/molL﹣1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为 .
(3)碳酸:H2CO3 , Ki1=4.3×10﹣7 , Ki2=5.6×10﹣11
草酸:H2C2O4 , Ki1=5.9×10﹣2 , Ki2=6.4×10﹣5
0.1mol/LNa2CO3溶液的pH0.1mol/LNa2C2O4溶液的pH.(选填“大于”“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是 . 若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是 . (选填编号)
a.[H+]>[HC2O4﹣]>[HCO3﹣]>[CO32﹣] b.[HCO3﹣]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣]
c.[H+]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣] d.[H2CO3]>[HCO3﹣]>[HC2O4﹣]>[CO32﹣]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3﹣H2CO3 , 当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象.